Технически основы операции при Роботизированной Xирургии похожи на лапароскопическую операцию. Таким образом, практический опыт в области передовых лапароскопических операций непосредственно важен и для успеха в роботизированной хирургии.
Хирургические процедуры в Роботизированной Xирургии проводятся с помощью манипуляторов, помещенных внутрь организма, и сопровождаются увеличением в 10-15 раз 3-мерных изображений высокого разрешения. Самое главное преимущество манипуляторов – это то, что они дают хирургу возможность выполнять операции с помощью тонких и мелких кончиков инструментов при увеличении 3-мерных изображений высокого разрешения без вибрации под углом 540°.

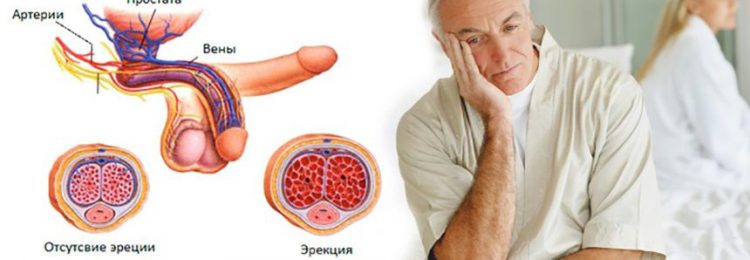
Как показано на рисунке, при радикальной хирургии рака простаты, после удаления простаты уретра сшивается к шейке мочевого пузыря на уровне наружного дефекта.
Каковы преимущества Роботизированной Хирургии в лечении рака простаты?ı
После «Роботизированной хирургии» продолжительность пребывания в больнице составляет 1 или 2 дня. Примерно 95% больных на второй день после операции выписываются из больницы.
- Небольшие кровопотери во время операции по сравнению с традиционной открытой хирургией. Следовательно, уровень переливания крови также очень низок (1-2% в роботизированной хирургии, 40-45% в открытой хирургии)
- Небольшая необходимость в применении обезболивающих на протяжении всего срока госпитализации, а также после выписки из больницы.
- Обычно мочевой катетер удаляется в течение первой недели после операции, если не возникает осложнений между 4 или 7 днями. Этот период в открытой хирургии обычно составляет 14-21 дней.
- Около 90% пациентов на 2-й или 3-й неделе после радикальной хирургии простаты с помощью Роботизированной Хирургии возвращается к своей обычной ежедневной активности.
Все детали нервосберегающего метода в Роботизированной Хирургии
Для проведения передовых лапароскопических операций с помощью инструментов для лапароскопической хирургии очень важны знания анатомического строения нервных и мышечных пучков простаты. Данный опыт вместе с преимуществом Системы Роботизированной Хирургии позволяют достичь самого высокого уровня эффективности нервосберегающей и мышцесберегающей операции.
Известно, что нерв идущий к пенису и обеспечивающий эрекцию при половом акте находится не в виде одного нерва, а в виде нервного пучка. Однако, исследования последних лет показали, что у 60% пациентов данный нервный пучок не находится в нижней боковой части простаты (Рисунок -1). Иными словами, при открытой хирургии многие врачи считают, что сберегают нерв идущий к пенису, однако на самом деле, у 60% больных повреждают нервный пучок в передней части простаты. Следовательно, вопреки ожиданиям, после операции у пациента развивается стойкая потеря эрекции. С помощью телескопа, установленного через пупок и экрана высокого разрешения (high definition) можно наблюдать за увеличенным в 10-15 раз изображением, а через другие отверстия, в которые установлены хирургические инструменты с острыми наконечниками, можно проводить операцию при сопровождении изображений всех тканей и различных анатомических структур. Сосудисто-нервные пучки у всех пациентов хорошо сберегаются с помощью хирургических инструментов с острыми наконечниками при сопровождении данного изображения. Роботизированная хирургия Да Винчи повышает данное преимущество лапароскопии еще на один уровень и обеспечивает доступ к ткани под 3-мерным и четким изображением с помощью кончиков манипуляторов внутри тела и движениями без вибраций под разными углами. На данном этапе самым главным является опыт хирурга в области общей лапароскопической хирургии перед использованием робототехники и частота применения хирургом данного метода в лечении рака простаты.
Рисунок-1b, как считалось раньше, нервный пучок находится в одной области только у 40% мужчин – полосатые стрелки.

Нервные пучки идущие к пенису у 60% мужчин простираются на передней поверхности простаты (Рисунок-1). По этой причине, поставлен вопрос о сбережении нервных пучков с помощью двух разных методов. Сбережение всей капсулы простаты со всеми мембранами (фасции) и нервных пучков между данными мембранами требует опыта и терпения. Этот метод называется ИНТРАФАСЦИАЛЬНЫМ НЕРВОСБЕРЕГАЮЩИМ ДОСТУПОМ (Рисунок-2: линия с синими полосками). Из-за образованных мембран и нервных пучков также называется «Завеса Афродиты». С помощью роботизированной системы Да Винчи данный метод обеспечивает 90-95% сохранности эрекции пениса. Тем не менее, уровень сохранности эрекции пениса в открытой хирургии составляет 51-60%.


Необходимо подчеркнуть, что функция удержания мочи у пациентов со сбереженными мембранами в виде Завеса Афродиты и нервного пучка, идущего к пенису восстанавливаются очень быстро, а уровень восстановления достигает 98%.
В итоге, с помощью технических преимуществ Роботизированной Системы Да Винчи и большого опыта хирурга в области лапароскопической хирургии обеспечивается высокий уровень сбережения нервов и сосудов идущих к пенису, а также продолжение сексуальной активности после операции.
Если желаете поделиться данными этой статьи с друзьями, опубликуйте ссылку на него на своей странице, выбрав кнопку нужной соцсети:
Источник www.kostyuk.ru
Тесная взаимосвязь психологического и физического состояния человека давно доказана. Многие болезни возникают или усугубляются на фоне стрессовых ситуаций. Это известная всем психосоматика, влияющая на функционирование организма. Она зачастую приводит к язве пищевода, мигрени, гипертонии, а также к проблемам предстательной железы у мужчин. Речь идет о так называемом нервном простатите, который развивается на фоне сбоев в работе центральной нервной системы.
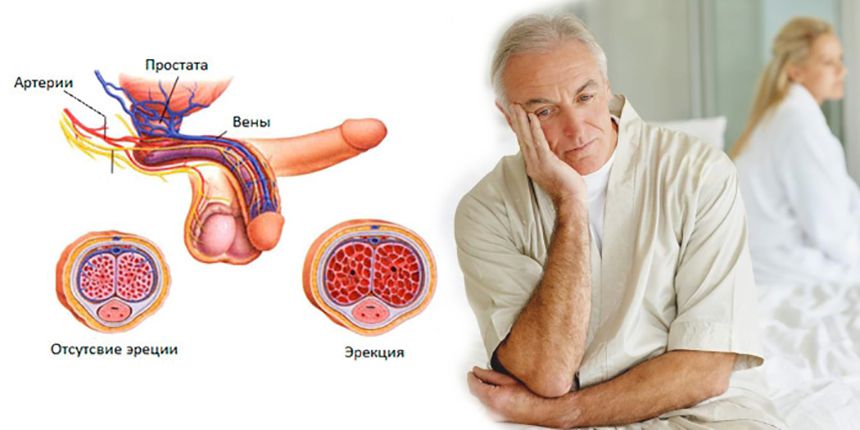 Проявление нервного простатита
Проявление нервного простатита
Что такое «нервный простатит»
Простатит является воспалительным заболеванием предстательной железы. Он носит инфекционный или неинфекционный характер. Последний как раз и возникает зачастую на фоне неправильного образа жизни и постоянных стрессов. Современный жизненный ритм этому способствует.
В медицине не существует термина «нервный простатит». Это обиходное название патологии, вызванной нарушениями в работе центральной нервной системы. Он объясняет не форму болезни, а ее причину – нервное перевозбуждение и эмоциональный стресс. Неблагоприятные психологические факторы сопровождают мужчину ежедневно, что и приводит в результате к физиологическим сбоям в организме.
Основными причинами возникновения болезни выступают:
- тяжелая, изнуряющая работа;
- семейные проблемы;
- плохой сон и бессонница;
- недостаток отдыха;
- эмоциональная напряженность;
- депрессивное состояние;
- раздражительность, вспыльчивость;
- проблемы сексуального характера.
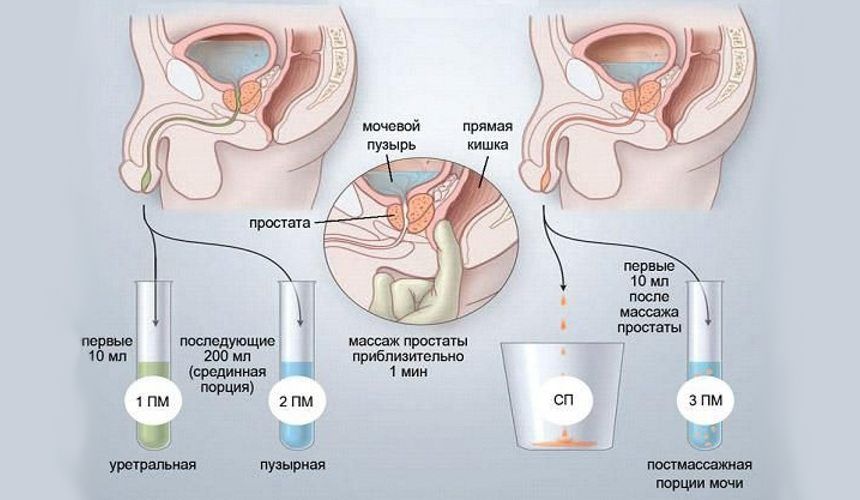 Забор анализов на простатит
Забор анализов на простатит
Длительное влияние этих факторов нарушает проводимость нервных импульсов от головного мозга к простате. Появляются реальные физические симптомы недомогания: дискомфорт в области промежности, сексуальная дисфункция, нарушение мочеиспускания, плохое самочувствие. Это, в свою очередь, приводит к развитию простатита или обострению хронической его формы. Постоянный эмоциональный перегруз чреват серьезными осложнениями не только со стороны простаты, но и сердца, сосудов, других органов и систем.
Механизм возникновения простатита из-за нервов
Психосоматические причины развития многих заболеваний носят абсолютно логичный и объяснимый характер. Нервная система человека работает по принципу импульсов, которые передаются от клеток к мозгу и наоборот. Когда этот механизм нарушается, возникают нейрогенные расстройства и сопутствующие им физиологические проблемы.
С точностью определить роль соматики в развитии воспаления предстательной железы невозможно, но предположить этот фактор можно с большой вероятностью. В частности, прослеживается два основных механизма влияния психологического состояния мужчины на функциональность простаты.
 Простатит: строение мочеполовой системы
Простатит: строение мочеполовой системы
- Первый механизм заключается в изначальном развитии острого, а затем хронического, простатита по причине перманентной перегрузки нервной системы. Это может быть тяжелая и ненормированная работа, сложные отношения в коллективе и семье, накопившаяся многолетняя усталость, неудовлетворенность в личной жизни, наличие серьезных личностных комплексов. В результате появляются неприятные ощущения в промежности, нарушается отток мочи, снижается половое влечение и либидо. На этом этапе важно остановиться и подумать об изменении ритма жизни и отношения к окружающей действительности. Своевременная реакция на тревожные сигналы вполне может предотвратить развитие патологии и восстановить мужскую силу.
- Второй механизм подразумевает так называемый порочный круг. При появлении у мужчины проблем с предстательной железой, сопровождающихся болезненными ощущениями и сексуальной дисфункцией, возникает замкнутый круг. Из-за своей несостоятельности мужчина испытывает постоянный стресс, психологическое неудобство, появляется раздражительность и нервозность. Работа нервных импульсов полностью переключается на переживания. В результате зацикленности на проблеме состояние здоровья еще больше ухудшается, болезнь усугубляется и осложняется, увеличивается количество рецидивов и острота симптомов. Таким образом, формируется круговая реакция, из которой можно выйти только благодаря нормализации нервно-психического состояния.
Спокойствие и эмоциональная стабильность – важные составляющие здоровья мужчины. Очень важно следить за психологическим состоянием и способом жизни, чтобы не допустить возникновение простатита или более серьезных патологий. Кроме того, не стоит забывать о своевременном обращении к врачу и лечении физиологических нарушений в предстательной железе.
Важные рекомендации
Непреложным является тот факт, что далеко не каждый случай простатита – результат психосоматических нарушений. Но нельзя отрицать, что эмоциональное состояние мужчины играет далеко не последнюю роль в развитии и осложнении патологии. Особенно если речь идет о городских жителях. По статистике уровень стресса у мужчин, проживающих в мегаполисе гораздо выше тех, кто обитает в сельской местности. Соответственно и риск проблем с мочеполовой системой возрастает многократно.
В отличие от физиологических изменений, работу центральной нервной системы можно успешно нормализовать, выполняя следующие рекомендации:
- своевременно лечить воспаление простаты, чтобы потом не бояться отсутствия результата от терапии на поздних стадиях;
- следить за режимом дня – не переутомляться на работе, хорошо питаться, достаточно отдыхать;
- научиться адекватно реагировать на стрессовые ситуации, возникающие в коллективе и семье;
- заниматься умеренными физическими нагрузками, которые существенно снижают реакцию на внешние раздражители;
- при необходимости посещать психолога или психотерапевта;
- выработать уверенность в себе и своих силах, в том числе сексуальных;
- не зацикливаться на существующих проблемах с простатой, а просто выполнять все рекомендации доктора.
Эти простые советы помогут не только быстро излечиться от недуга, но и предотвратить появление на нервной почве простатита. Берегите нервы и будьте здоровы!
Originally posted 2017-11-27 11:13:54.
Источник prostatoff.ru
Иннервация простаты осуществляется симпатическими, парасимпатическими и соматическими нервами. Симпатические нервы исходят из Th11—L2 и представляют собой верхнее гипогастральное сплетение, откуда нервные волокна направляются к нижнему гипогастральному сплетению.
Парасимпатическая иннервация осуществляется зоной S2—S4, которая формирует нижнее гипогастральное сплетение. Последнее содержит как парасимпатические, так и симпатические нервы и располагается сбоку и спереди от прямой кишки. Нейроваскулярный пучок локализуется постлатерально, у основания простаты, иннервируя фасции Денонвиллье и тазовую. Соматические нервы также исходят из S2-S4 и иннервируют поперечно-полосатую мускулатуру таза и уретрального сфинктера (рис. 13, 14).

Рис. 13. Пространственное изображение нейроанатомии таза, мочевого пузыря и предстательной железы (по A.Tewari et al., 2003)
Таким образом, строма и гладкая мускулатура простаты покрываются сетью холинергических и адренергических нервов. На границе между латеральной и задней поверхностями простаты перипростатическая фасция включает два-три нервных пучка, проходящих параллельно простате и заканчивающихся в кавернозных телах полового члена. Разветвленные верхние и нижние пучки нервов распространяются в латеральных отделах фасции Денонвиллье. Большая часть самой простаты иннервируется верхним нервным пучком, отдающим дорсолатерально три ветви в области основания простаты от сосудисто-нервного пучка.

Рис. 14. Половой нерв и его ветви, осуществляющие иннервацию полового члена и наружного сфинктера
Отдельные маленькие ветви обеспечивают иннервацией верхушку простаты. Автономные ганглии расположены непосредственно вблизи сосудисто-нервных пучков либо в перипростатической жировой ткани, где образуют цепочку на поверхности предстательной железы, проникают сквозь капсулу и заканчиваются в ее паренхиме.
Особого внимания заслуживают нейроваскулярные пучки, проходящие симметрично вдоль нижнебоковых поверхностей предстательной железы и тесно с ней связанные. Значение этих структурных образований важно в двух аспектах:
- опухолевая инвазия происходит вдоль капсулы по периневральным пространствам этих пучков. Прежде всего на верхушке и у основания простаты обнаруживаются пенетрирующие капсулу нервы;
- повреждения пучков во время радикальной простатэктомии вызывают расстройство сексуальной функции. Поскольку они ответственны за нормальное состояние эрекции, их сохранение при простатэктомии приобретает особо важное значение. Частичное повреждение или двустороннее пересечение нервно-сосудистых стволов почти всегда сопровождается нарушением эректильной функции или ее полной потерей.
Предстательная железа, семенные пузырьки и бульбоуретральные железы являются внутренними мужскими половыми органами, физиологическое предназначение которых точно не известно. По крайней мере, современные знания позволяют оценить их функцию как необходимую для разжижения и сохранения функциональности спермы. Однако роль «семенной жидкости», в составе которой имеются простагландины, спермины, цинк, протеаза, эстераза, фосфатаза и многие другие компоненты, продолжает активно изучаться.
Гормональная регуляция роста и функции предстательной железы
Нормальная функция предстательной, равно как и других мужских половых желез, обеспечивается андрогенами яичкового и надпочечникового происхождения. Многогранность взаимодействия андрогенов с эпителием простаты, ее стромальным компонентом, нейроэндокринными клетками, одновременно циркулирующими другими гормонами (в частности эстрогенами), факторами роста представляет сложную систему, осуществляющую регуляцию как роста самой простаты, так и баланс относительного количества и функции эпителиальных и стромальных клеток. Однако этим не исчерпываются их взаимоотношения, поскольку оптимальный баланс возможен только при определенных соотношениях в продукции факторов роста.
Для четкого восприятия всего многообразия эндокринных взаимоотношений целесообразно условно выделить центральное регуляторное звено и процессы, которые происходят на уровне самой предстательной железы. P.Davies и C.L.Eaton (1991) показали, что гипоталамус, гипофиз и гонады (яички) включены в эндокринную «петлю», которая ответственна за поддержание адекватных уровней стероидных гормонов в сыворотке и тканях-мишенях (рис. 15).

Рис. 15. Схематическое изображение роли гипоталамо-гипофизарно-гонадной оси при росте простаты
Упрощенная схема гормональной регуляции роста предстательной железы хорошо известна. Андрогены непосредственно участвуют в регуляции клеточного роста как в нормальных условиях, так и при развитии патологического процесса — рака предстательной железы. Основную регуляцию уровня андрогенов в крови обеспечивает упомянутая гипоталамо-гипофизарно-гонадная «петля» эндокринной системы. Прежде всего в гипоталамусе в пульсирующем режиме секретируется декапептидный лютеинизирующий гормон рилизинг-гормона (ЛГРГ), который стимулирует выделение передней долей гипофиза двух основных гормонов.
Первый из них — лютеинизирующий — активизирует и стимулирует секрецию лютеинизирующего гормона передней доли гипофиза. Продукция тестостерона непосредственно происходит именно под воздействием лютеинизирующего гормона в яичках. Тестостерон, в свою очередь, также оказывает регулирующее действие на продукцию лютеинизирующего гормона путем отрицательного обратного воздействия на гипоталамус и гипофиз. Другой гормон гипофиза — фолликулостимулирующий — оказывает специфическое действие, стимулируя сперматогенез.
Рецепторы для этих гормонов найдены и в простате. Самостоятельная линия стимуляции мужского полового гормона осуществляется под влиянием адренокортикотропного гормона на синтез в надпочечниках андростендиона и дигидроэпиандрестерона, которые последовательно превращаются в тестостерон путем локальной и периферической конверсии. Более 95% циркулирующего тестостерона находится в крови либо с глобулином, связывающим половой гормон (секс-гормонсвязывающий глобулин), либо с альбумином. Только несвязанная фракция — около 3 % свободно циркулирующего тестостерона — может попасть в клетки мишени простаты путем диффузии, где и включается в разнообразные стероидные метаболические этапы, которые совершаются в ходе активной регуляции (J. Е. Damber et al., 1983).
Наиболее важный шаг — это конверсия в дигидротестостерон (ДГТ). Оба вида параллельных андрогенов (яичковые и надпочечниковые) проникают в цитоплазму клеток предстательной железы, где под воздействием 5а-редуктазы, ферментативной системы, локализованной на ядерной мембране, превращаются в дигидротестостерон, который соединяется со специфическими рецепторами, и образовавшийся комплекс проникает в ядро клетки, активизируя синтез ДНК (рис. 16). Дигидротестостерон, связанный с внутриклеточными андрогенорецепторами, приобретает выраженную активность, что способствует ядерному перемещению (транслокации) сформировавшегося стероид-рецепторного комплекса (W. I. Mainwaring, 1977). Последний контролирует регуляцию клеточного цикла, клеточный рост и дифференциацию.

Рис. 16. Тестостероновая поддержка функции простатических клеток и стимуляция клеточного роста
Рецептор человеческого андрогена — это 110 кДа-протеин, который расшифровывается однокопийным геном, расположенным на Х-хромосоме. Активированный стероид представляет собой рецепторный комплекс, который имеет домен (область) высокого сродства с избирательными хроматиновыми сайтами является модулятором генной экспрессии в клетках предстательной железы (W. Т. Schrader, 1984).
Предстательная железа находится не только под эндокринным контролем, гомеостаз органа поддерживается и другими регуляторными факторами. Существующие нейроэндокринные клетки по своей природе секреторные, могут оказывать аутокринно-паракринное действие. Это разновидность эпителиальных клеток простаты, которые могут взаимодействовать паракринным образом со стромой (G.Aumuller et al., 1999). Паракринная коммуникация по сути является локальной, ограниченной связью с рецепторами прилежащих клеток.
Аутокринные секреции стимулируют сами клетки, которые и секретируют их. В нормальных условиях аутокринные секреты не попадают в общую циркуляцию (P.A.Abrahamsson, 1999). Считается, что через разнообразные секреторные продукты они формируют коммуникационную сеть, участвующую в клеточной регуляции.
Важное значение имеет также выяснение роли андрогенов в реакциях роста, его факторах и рецепторах факторов, клеточных протоонкогенов. К настоящему времени накоплены убедительные доказательства, подтверждающие вовлечение тканевых факторов роста в процесс прогрессирования рака простаты (G.O.Hellawell, S.F.Brewster, 2002). Факторы роста регулируют развитие клеток, их дифференциацию и апоптоз (программированную клеточную смерть). Их семейство довольно многочисленно, а функциональное приложение разнообразно и нередко является прямо противоположным как в нормальной предстательной железе, так и при развивающемся в ней раке (табл.1).
Факторы роста действуют на прилежащие стромальные клетки паракринным образом и связаны с регуляцией эпителиальной пролиферации. Примером разнонаправленного действия факторов роста могут служить две группы. Так, группа факторов роста фибробластов (FGF), в которую входят инсулиновый фактор роста IGF, эпидермальный EGF и трансформирующий фактор роста TFG-а, а также факторы эндотелиального роста (фактор роста, извлеченный из тромбоцитов, — PDGF и фактор сосудисто-эндотелиального роста — VEGF), — главные стимулирующие регуляторы пролиферации в простате. Группа TGF-В является ведущим ингибитором пролиферации. Факторы роста оказывают аутокринный и паракриннный эффекты на стромальные и эпителиальные клетки, взаимодействуют с другими факторами и связующими протеинами для регуляции роста простаты (рис.17).

Рис. 17. Факторы роста и их рецепторы, вовлеченные в нормальное развитие простаты (по R. Byrne etal., 1996)
В. Djayan et al. (1999) показали, что высокий уровень инсулиноподобного фактора роста IGF-1 сочетается с большим риском развития рака простаты. Они подтвердили, что увеличение уровня IGF-1 на 7-8% отмечается у больных раком простаты. Хотя эти значения не зависят от уровня ПСА, вычисляемое отношение IGF-1/ПСА повышает специфичность установления рака предстательной железы, причем основным параметром является уменьшение соотношения.
Таблица 1. Факторы роста в нормальной простате и при раке (по G. О Hellawell и S.F.Brewster. 2002)

R. Kurek et al. (1998) относя IGF-1 к новым диагностическим параметрам, провели сравнительную оценку количественных показателей у пациентов с гиперплазией и раком предстательной железы. В первой группе среднее значение IGF-1 составило 62,5 мг/л, в то время как во второй оно было 110 мг/л. Наиболее высокие значения (до 350 мл/л) констатировались у больных раком простаты в стадии рТЗ с N+, МО. Авторы поддерживают тезис о каузальной связи между высоким содержанием IGF-1 в сыворотке крови и достоверностью рака простаты.
Механизм такой закономерности объясняется отчетливым пролиферативным влиянием IGF-1 на эпителиальные клетки. Интересен и лечебный подход основанный на тепловом воздействии, что вызывает уменьшение уровня IGF-1 и 60%-ную редукцию раковых клеток (W.E.Sonntagetal.,1999).
Нельзя не отметить и роль эстрогенов в процессах гормональной регуляции клеточных взаимоотношений предстательной железы. Концентрация плазматических эстрогенов у мужчин более низкая, чем тестостерона, значительная часть их аккумулируется в жировой ткани. Установлено, что 75-90% плазматических эстрогенов у молодых здоровых мужчин — это продукты периферического метаболизма (ароматизации) андростендиона и тестостерона в эстрон и эстрадиол. Суточная продукция эстрадиола у мужчин составляет 40мкг. Помимо периферического синтеза, источником секреции эстрогенов в мужском организме являются яички, что подтверждается признаками феминизации мужчин при опухолях клеток Сертоли и указывает на их участие в синтезе эстрогенов.
Взаимодействие двух гормонпродуцирующих клеток яичка — Лейдига и Сертоли — обеспечивает синтез эстрогенов, поскольку клетки Сертоли в противоположность клеткам Лейдига не утилизируют прегненолон как субстрат для ароматизации эстрогенов. У здоровых мужчин пожилого возраста и пациентов с аденомой предстательной железы происходят усиление секреции эстрогенов и параллельно морфо-функциональные изменения в клетках Сертоли, гистохимическая характеристика которых отражает их повышенную секреторную активность. Процесс протекает под контролем фолликулостимулирующего гормона (ФСГ), по отношению к которому клетки Сертоли являются мишенями, что подтверждается присутствием специфических ФСГ — рецепторов на мембранах клеток Сертоли.
Предполагается, что ФСГ регулирует синтез спектра стероидов, находящихся в канальцах, и путем изменения концентрации андрогенсвязывающих протеинов оказывает влияние на превращение тестостерона в эстрадиол. В связи с этим получила разработку концепция единой тестостерон-эстрогенной секреторной системы яичек, морфофункциональную основу которой составляют оба типа гормонпродуцирующих клеток яичка. Некоторые морфологические и функциональные изменения в предстательной железе удается наблюдать у орхиэктомированных лабораторных животных при введении им эстрогенных препаратов, что указывает на их чувствительность. Об этом же свидетельствует присутствие эстрогенных рецепторов в отдельных клеточных кланах с преобладанием в центральной части железы — так называемой мужской маточке.
У пожилых мужчин возрастает тестикулярная продукция эстрогенов. На фоне умеренного снижения уровня андрогенов в системной циркуляции это приводит к сдвигу андроген-эстрогенного баланса в сторону женских половых гормонов. При достаточной выраженности таких сдвигов они могут стать причиной возрастной склеротической атрофии предстательной железы.
В физиологических концентрациях эстрогены не оказывают непосредственного влияния на клетки рака предстательной железы. Первичное действие эстрогенов при лечении этого вида опухоли основано на их системном действии и заключается в подавлении эстрогенами синтеза и высвобождения ЛГРГ в гипоталамусе, что ведет к понижению секреции лютеинизирующего гормона (ЛГ) и, таким образом, к резкому уменьшению продукции тестостерона в яичках (A. A.Sandberg 1980). In vitro был продемонстрирован непосредственный ингибирующий эффект эстрогенов на высвобождение тестостерона из клеток Лейдига в яичках (L.Daehlin et al., 1985).
Последние, вероятно, необратимо повреждаются после долгосрочного лечения эстрогенами, что приводит к нарушению продукции тестостерона, которое продолжается и после отмены эстрогентерапии (R.Tomic et al., 1988). Оральные эстрогены вызывают повышение уровня глобулина, связывающего половой гормон в крови, что обусловливает снижение биологически активного свободного тестостерона в сыворотке крови (G.E.Damber et al., 1983). При этом проявляется эффект, сходный с действием максимальной андрогенной блокады. Эстрогены обладают также некоторым действием на адренальный стероидогенез, понижая уровни адренальных андрогенов предположительно путем изменения печеночной функции (R.Stege et al., 1988).
Кроме влияния тестостерона на простату, эстрогены и прогестины взаимодействуют также с этой железой. Эстрогены конкурируют за участки контакта с секс-глобулинсвязывающим гормоном, с которым тестостерон как доминантный стимул роста простаты, весьма активно связывается, хотя тестостерон проявляет благосклонность к этому протеину. Из-за их взаимодействий у мужчин в возрасте 50-60 лет констатируется 40%-ное повышение в соотношении свободного эстрадиола к свободному тестостерону. Основное влияние эстрогенов на предстательную железу может осуществляться через систему гипоталамус-гипофиз, которая является конечным органом, оказывающим подавляющее действие на тестикулярный синтез тестостерона.
В эксперименте показано, если эстрогены и тестостерон вводятся кастрированным животным одновременно, то у них происходит нормальный рост предстательной железы, а значит эстрогены не блокируют эффект замещения введенного тестостерона. Возможен и такой вариант: пролактины играют особую роль в росте и метаболизме предстательной железы. Рецепторы пролактина обнаружены в предстательной железе, яичках и могут выступать посредниками пролактина при поглощении тестостерона и метаболизме в простате.
В какой-то мере эффект воздействия эстрогенов подобен аналогам лютеинизирующего гормона рилизинг-гормона, хотя первые подавляют образование лютеинизирующего гормона, а вторые препятствуют его выделению. Тонкости этих процессов недостаточно выяснены, но зато четко обрисовывается токсичность эстрогенов с выраженным негативным эффектом для сердечно-сосудистой системы. Эстрогены могут также подавлять функцию клеток Лейдига. Эффект кастрации весьма существенен, поскольку приводит к резкому снижению уровня тестостерона плазмы, обычно от первоначального диапазона (500—600 нг/мл) до менее чем 50 нг/мл, что вызывает ощутимое подавление роста нормальной и раковой ткани простаты.
Источник medbe.ru