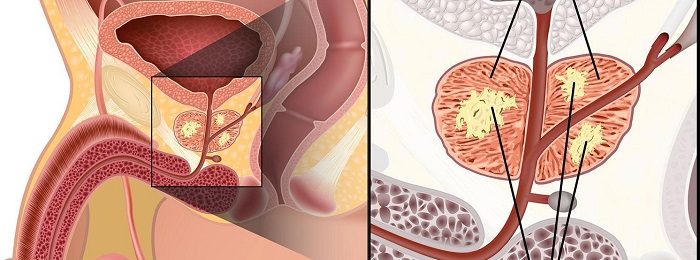
Патофизиологические механизмы гормоноризистентности при раке предстательной железы
— гормональнозависимая опухоль, и чтобы понять механизм развития гормопорезистентных форм при РПЖ, важно уяснить взаимодействие гормонов в
Современные научные представления свидетельствуют о достаточной изученности патофизиологических механизмов гормонорегуляции в экспериментальной и клинической практике.
Тем не менее фундаментальные механизмы, ведущие к развитию гормонорезистентного рака предстательной железы (ГРПЖ), не полностью ясны.
Известно, что необходимы многочисленные события дли трансформации клеток в злокачественные, и хотя последовательность этих событий недостаточно исследована, установлено, что они происходят как во время транскрипции темой, так и после нее.
В наиболее тяжелом положении оказывается группа больных, у которых на фоне проводимой гормональной терапии (ГТ) клинический эффект отсутствует либо бывает незначительным.
Классификация рака простаты
Верная классификация рака предстательной железы проводится по нескольким системам:
- по строению клеток (для оценки агрессивности роста и развития опухоли);
- по степени дифференцировки опухолевых клеток (насколько похожи раковые клетки на здоровые, из которых они развились);
- по уровню распространения опухоли в организме человека (система TNM).
Гистологическая оценка — шкала Глисона
Этот вид классификации предложил американский патоморфолог Дональд Глисон. В 1974 году после ряда проведенных исследований и изучения свойств биологического материала он сформулировал шкалу степеней злокачественности рака.
Степень дифференцировки опухоли разделяют на пять частей:
- Опухоль состоит из маленьких однородных желёз с ядрами, изменёнными минимально.
- Многочисленные скопления желёз, которые располагаются близко друг к другу, но все ещё разделены.
- Клетки имеют разную форму и размеры, прорастают в окружающие ткани.
- Много явно атипичных клеток с прорастанием в окружающие ткани.
- Слои не дифференцированных атипичных клеток.
Индекс Глисона состоит из суммы двух цифр, которые присваивают изученной биопсии (тканевой пробе). Каждая из составляющих оценивается по шкале от 1 до 5 баллов. В зависимости от суммы будет присвоена оценка опухоли.
Рассмотрим пример. Для исследования у пациента берут два образца ткани предстательной железы и каждому образцу присваивают балл.
Самый низкий балл обозначает нормальное состояние клеток, а самый высокий – 5 баллов – говорит об агрессивном раке. Сумма этих образцов и будет составлять индекс Глисона. 2 3=5. Первая цифра – это раковые клетки в простате, а вторая – это нормальные клетки. И чем выше первая цифра, тем агрессивнее опухоль. Худший результат – это 5 5=10.
Система TNM
Система TNM– это международная систематизация злокачественных новообразований, разработанная Пьером Денуа. Буквы являются аббревиатурой латинских слов Tumor(опухоль), Nodus(узел, имеются в виду лимфоузлы), Metastasis(метастазы).
ВАЖНО! С помощью этой системы определяют уровень распространенности рака в простате (индекс Т), количество пораженных раком близлежащих лимфоузлов (индекс N) и наличие или отсутствие метастазов в других органах и тканях (индекс M).

К этим трём буквам добавляют цифры, которые указывают на распространение опухоли: Tx, T0, T1, T2, T3, T4, Nx, N0, N1, Mx, M0, M1. Если есть сомнение в том, насколько правильно определена категория, то всегда выбирают наименее распространённую. Тоже касается и группировки стадий.
Классификация рака простаты по системе ТНМ:
- Т1N0M0 или Т2N0M0 когда опухоль находится только в предстательной железе, нет метастазов, прогноз хороший.
- Т2N1M0 или Т2bN0M0 опухоль ограничена пределами органа, метастазы в регионарных лимфоузлах, прогноз осторожный.
- Т3N2M0 или Т3N1M0 опухоль увеличилась в размерах с прорастанием в окружающие ткани, есть метастазы в прилежащие лимфоузлы. Прогноз неблагоприятный.
- Т4N0M0 или Т4N3M1 размеры и расположение опухоли достаточно распространенные и возможные отдаленные метастазы. Опухоль неоперабельна и прогноз очень неблагоприятный.
Гормонозависимый и гормононезависимый
Рак предстательной железы в своем большинстве является гормонозависимым, так как простата вырабатывает мужской половой гормон тестостерон, который стимулирует не только рост клеток простаты, но и рост раковых клеток. Поэтому лечение такого вида рака основывается на подавлении уровня тестостерона другими гормонами.
Гормонорезистентный рак предстательной железы — это рак, который прогрессирует в течение 12 – 18 месяцев, несмотря на то что уровень тестостерона достаточно низок.
Гормональная терапия в этом случае является неэффективной, потому что раковые клетки становятся устойчивыми к ней. Почему так происходит, до сих пор непонятно.
Гормонозависимый и гормононезависимый рак простаты разница: выживаемость после развития гормононезависимого рака ниже чем у гормонозависимого и наиболее эффективным способом лечения в данном случае будет являться химиотерапия.
Все методы классификации рака предстательной железы разработаны для подбора необходимой методики лечения. При проведении любого вида лечения пациент должен быть предупрежден об осложнениях, сопутствующих этому лечению, и он вправе будет выбирать что ему больше подходит. Ваше здоровье — в ваших руках.
Признаки и симптомы

На начальных стадиях заболевание может протекать без каких-либо симптомов. Поэтому стоит прислушиваться к любым негативным изменениям, происходящим в организме.
Основные симптомы и признаки:
- частое затрудненное и болезненное мочеиспускание;
- слабый напор и прерывистость при мочеиспускании;
- присутствие крови в моче и сперме.
Методы лечения гормонорезистентного рака предстательной железы
Считают, что резистентность к ГТ рано или поздно развивается у любой опухоли, однако не все больные доживают до этого момента. Переход к гормонорезистентному раку клинически характеризуется нарастанием содержания ПСА и прогрессированием заболевания на фоне проводимой ГТ. В такой ситуации необходимо скорректировать проводимую гормонотерапию или перейти к следующей линии препаратов.
Обнадеживающие результаты применения альтернативных схем лечения были получены в ходе клинических исследований II фазы, в которых применяли пегилированный доксорубицин, комбинацию паклитаксела, карбоплатина и эстрамустина, комбинацию винбластина, доксорубицина и радионуклидов и комбинацию доцетаксела и митоксантрона.
Отсутствие репрезентативных рандомизированных исследований III фазы и данных о долговременном эффекте терапии — основные проблемы, связанные с этими исследованиями.
.
Циклофосфамид для приема внутрь
Внутривенное применение циклофосфамида было изучено в ходе многих исследований. Однако сейчас большой интерес вызывает возможность приема циклофосфамида внутрь. Такой метод менее токсичен, чем внутривенное введение, и может оказаться более эффективным. Исследование по применению пероральных циклофосфамида и этопозида у 20 пациентов дало обнадеживающие результаты.
Цисплатини карбоплатин
Несмотря на разнообразие проводимых неследований, для постоянно растущего количества больных ГРПЖ необходимы разработка и адаптация новых стратегий, ведущей из которых остается лекарственная терапия.
1. Симптоматический эффект гормональных препаратов, стабилизация заболевания на фоне их приема максимум па 2-4 мес.
2. Возможности применения гормонотерапии преимущественно в комбинациях с химиопрепаратами, из которых наиболее активными в настоящее время являются таксаны, в частности доцетаксел. В последнее время вновь возрос интерес к эстрогенам как виду терапии ГРПЖ.
3. Эффективность применения химиопрепаратов как в режиме монотерапии, так и в комбинации.
По сравнению с режимами лечения, используемыми в 80-е и 90-е годы XX века, новые препараты выводят химиотерапию на одно из ведущих мест в лечении ГРПЖ. Эти режимы демонстрируют ответ по ПСА как основному маркеру заболевания, ответ со стороны «измеряемого заболевания» — то есть стабилизацию или регрессию процесса по пораженным лимфатическим узлам, другим участкам метастазирования в паренхиматозные органы и мягкие ткани.
Современные химические агенты увеличивают время ОВ. Следует отметить как менее существенный фактор — период до прогрессирования заболевания на фоне лечения. Это обусловлено тем, что зачастую при минимальном времени до прогрессирования происходит значительное увеличение ОВ.
Важен также положительный эффект со стороны вовлеченных в патологический процесс костных тканей, что проявляется снижением накопления реитгепфармпрепарата при сцинтиграфическом исследовании костей и, что самое главное для этой категории больных, — снижением градации боли.
В свою очередь, данные эффекты повышают качество жизни больного, что при паллиативной направленности проводимого лечения играет немаловажную роль. В РФ в настоящее время основным методом лечения ГРПЖ остается цитотоксическая терапия.
Однако ни один из существующих режимов не показал преимущества в ОВ и продолжительности жизни больных ГРПЖ. Таким образом, поиск и разработка наиболее эффективной схемы лечения ГРПЖ остается на сегодняшний день одной из актуальных задач, стоящих перед онкологами и урологами.
П.В. Глыбочко, Ю.Г. Аляев
Гормонотерапия второй линии
Возможность развития андрогеннезависимого
свидетельствует о том, что болезнь может прогрессировать даже после кастрации.

Кастрационный уровень тестостерона должен быть документально зафиксирован, так же как уровень тестостерона в сыворотке крови
Источник prostatitnik.ru

-
Содержимое:
- Почему рак простаты становится гормонорезистентным
- Чем опасен переход в гормононечувствительное состояние
Применение гормонотерапии, лечения, блокирующего выработку тестостерона, существенно замедляет процесс развития ракового заболевания. Со временем назначаемые препараты теряют эффективность. В тяжелых случаях диагностируется гормонорезистентный рак предстательной железы, продолжающий активно прогрессировать, несмотря на низкий уровень тестостерона в крови.
Почему рак простаты становится гормонорезистентным
Гормонорефрактерный рак предстательной железы диагностируют в том случае, когда онкология продолжает прогрессировать в течение 12-18 месяцев, несмотря на низкий уровень тестостерона в крови.
Европейская ассоциация онкологов разработала критерии оценки заболевания:
- Кастрационный уровень содержания тестостерона в крови 1,7 нг/моль.
- Последовательное повышение ПСА с интервалом не более 7 дней и дифференцированным 50% увеличением уровня простат специфического антигена на 50%.
- Устойчивая прогрессия ПСА, несмотря на применение различных тактик гормонотерапии.
Один из характерных признаков заболевания – уровень простат антигена в крови. Появление инструментальных видов исследований, позволяющих определить уровень ПСА сделало диагностику более достоверной. Уровень антигена при гормон-независимом раке простаты постоянно растет, даже несмотря на полную андрогенную блокаду.
Чем опасен переход онкологии простаты в гормононечувствительное состояние

Второй тип онкологии поддается терапии, первый нет. Гормонорезистентный рак имеет низкий порог выживаемости. Прогнозируемое продолжение жизни всего 2-3 года.
Как лечить гормононечувствительный рак простаты
Лечение гормонорефрактерного рака предстательной железы в отличие от резистивного подвида возможно, хотя и представляет некоторые сложности. Продолжают андрогенную блокаду. При достижении первичной гормонорезистентности назначают химиотерапию, рекомендуют проведение современных альтернативных методик.
Были разработаны схемы терапии, подбираемые по нескольким основным критериям:
- Устойчивость пациента к первой линии лечения.
- Выполнение полной андрогенной блокады.
- Индивидуальные особенности пациента.
Исходя из трех критериев отбора, лечащий врач подберет гормональную терапию, подходящую для каждого пациента в отдельности.
Использование гормонотерапии

Первая линия лечения гормононечувствительного рака простаты направлена на 1-2 группу клеток. Через время наступает устойчивость онкозаболевания к медикаментозной терапии. Подавление 1-2 группы тканей приводит к развитию раковой опухоли, состоящей исключительно из клеток, не требующих гормонов для роста и выживаемости.
Онкозаболевание для формирования перестает нуждаться в тестостероне. Развивается вторичная гормонорезистентность. На этом этапе гормонотерапия становится полностью неэффективной. Назначается химия.
Лечение химиотерапией
Раньше считалось, что химиотерапия, по причине своей низкой эффективности, существенно уступает другим методикам лечения раковых заболеваний. На данный момент были разработаны препараты, способные существенно облегчить состояние пациента, улучшить качество его жизни.
Несмотря на эффективность современной химиотерапии, пациенту оказывается исключительно паллиативное лечение, полного исцеления от онкозаболевания не наступает. Критерием эффективности считается продление жизни на 2-3 года.

Революционные методики терапии
Последние достижения в лечении позволили использовать в борьбе с онкозаболеванием собственную иммунную систему пациента. В Израильских клиниках был разработан метод использования вакцины против рака, не имеющий аналогов в мире.
Иммунотерапия практически не имеет побочных эффектов и отличается хорошей результативностью.
Методика проводится следующим образом:
- Берется забор крови у пациента.
- Клетки очищаются и обрабатываются синтетическими составами.
- Видоизмененная кровь вводится обратно, провоцируя борьбу с раковыми клетками.
Иммунотерапия в Израиле уже перестала быть экспериментальным лечением и входит в курс терапии крупнейших клиник. В России методика не применяется.
Как избежать кастрационно-рефрактерного рака простаты после гормонотерапии
Кастрационно-резистентный рак предстательной железы развивается, несмотря на тщательное планирование стратегии лечения и грамотно назначенный прием медикаментов. Причин этому несколько:
- Сроки возникновения гормонорезистентности оставляют всего 12-18 месяцев.
- Около 30% пациентов отказываются от проведения полной андрогенной блокады (орхиэктомия + гормонотерапия).
- Малая эффективность традиционных препаратов, относящихся к первой линии лечения.
- Недостаток гибкости в назначаемой терапии.
Схема современных методов лечения гормонорезистентного рака простаты, практикуемая в крупнейших клиниках Израиля, состоит в индивидуальном подборе лекарственных средств и постоянной корректировке назначаемых препаратов. Проводятся тесты с целью выявить привыкание раковой опухоли к воздействию медикаментов.
Выбор тактики лечения при кастрационно-резистентном раке предстательной железы связан в первую очередь с состоянием пациента и клиническими проявлениями злокачественных тканей. Только после полного обследования больного можно подобрать соответствующий вид лечения, включая современные методы борьбы с онкозаболеваниями.
Распространенность гормонорезистентного рака среди взрослого мужского населения (после 50 лет) занимает первое место. По мере старения организма, вероятность развития патологии увеличивается до 60-75%, что делает этот вид онкологии одним из самых опасных в мире.
Источник ponchikov.net
Статьи Комментарии
| »» Содержание | Б.П. Матвеев, Б.В. Бухаркин, В.Б. Матвеев |
Глава 10. Вторая линия эндокринной терапии рака предстательной железы и лечение гормонорезистентного рака предстательной железы
Наиболее сложная проблема в лечении рака предстательной железы возникает при наступлении, так называемой, вторичной гормонорезистентности, или в тех 15-20% случаях, когда опухоль первично резистентна к гормональному лечению. По мнению проф. А.М. Гарина (1997), самый тяжелый период в жизни больных распространенным раком предстательной железы наступает с момента прогрессирования на фоне максимальной андрогенной блокады или антиандрогенного подавления тестикулярного тестостерона. Здесь их жизнь измеряется уже месяцами.
Принципы второй линии терапии рака предстательной железы основываются на следующих постулатах. Фенотипически опухолевые клетки в предстательной железе состоят из 3 типов:
а) андрогензависимые (для продолжения их роста и выживания требуется андрогенная стимуляция). Такие клетки погибают при андрогенной блокаде;
б) андрогенчувствительные, они не погибают при отсутствии андрогенов, но их рост при этом ослабляется;
в) андрогеннезависимые — для их роста не требуются андрогены и они продолжают пролиферировать (Isaacs J.Т. et al., 1992).
Таким образом, андрогенная блокада приводит лишь только к элиминации андрогензависимых опухолевых клеток.
Широкое применение эстрогенов, как препаратов второй линии гормонотерапии, обусловлено тем, что многие авторы считают, что эстрогены обладают прямым цитотоксическим действием на клетки рака предстательной железы. В связи с этим, считается оправданным использование высоких доз эстрогенов, несмотря на возможность побочных действий.
Если после прекращения действия андрогенной блокады уровень сывороточного тестостерона остается выше кастрационного, то не все эндокринные возможности исчерпаны. Известно, что прогестины подавляют гонадотропины и тормозят превращение тестостерона в активный внутриклеточный дериват дигидротестостерон, они также конкурируют с андрогенами за рецепторы. Эффект при применении препаратов прогестинового ряда может быть получен у 15-20% больных. На заседании Американского общества клинической онкологии (ASCO) в 1998 г. в сообщении Dawson N.A. приведены данные об исследовании двух доз мегестрол ацетата — 160 мг и 640 мг. Объективный ответ в виде снижения уровня ПСА был достигнут у 12% пациентов, причем зависимости эффект — доза выявлено не было.
Выраженного субъективного эффекта в 20% наблюдений удается добиться от применения аминоглютетимида, создающего ситуацию медикаментозной адреналэктомии. Аминоглютетимид нарушает превращение холестерола в прегненолон, блокируя 20-24 десмолазу. При этом во избежание аддисонова криза необходимо одновременное назначение кортикостероидов. Однако по данным, приводимым Mahler Ch., (1997), значимого увеличения выживаемости не отмечено. Низкие и средние дозы стероидов подавляют надпочечниковые андрогены. Симптоматический эффект описан у 60% больных после применения дексаметазона в дозе 0.75 мг 2 раза в день. Одновременно отмечается снижение уровня ПСА более чем на 50% у большинства больных. В 30% имеются доказательства рентгенологического улучшения. Выживаемость составляет 6-9 месяцев.
Представляют интерес сообщения об определенной эффективности высоких доз кетоконазола. Кетоконазол — антигрибковый препарат, который нарушает функционирование цитохрома Р 450, и тем самым, угнетает надпочечниковый и тестикулярный синтез андрогенов. Применяются дозы 800-1200 мг в день. Первые исследования продемонстрировали объективный эффект в 16% и стабилизацию в 30% наблюдений. В некоторых сообщениях приводятся данные о снижении уровня ПСА на 90% у 50% больных. Описаны даже полные ремиссии продолжительностью до года. В более поздних исследованиях сообщается о средних сроках длительности ремиссии в 8.5 месяцев и медиане выживаемости — 19 мес. (Small E.J. et аl., 1997). Побочные действия кетоконазола проявляются в виде слабости, сонливости, тошноты, рвоты и снижения либидо. Заслуживают внимания сообщения о сочетании кетоконазола с адриамицином, которое вызывает снижение уровня ПСА более 50% у 57% пациентов гормонорефрактерным раком предстательной железы (Stemberg С.N., 1998). В настоящее время проводятся рандомизированные исследования нового деривата имидазола — Лиарозола, обладающего меньшим количеством побочных действий.
Описывается эффект повышенных доз тамоксифена у гормонрезистентных больных. Этот эффект отмечался при дозах 80 мг/м 2 х 2 раза в день у 38% пациентов, ремиссия продолжалась несколько месяцев.
Определенный интерес представляет, так называемый, синдром отмены антиандрогенов. У пациентов, прогрессировавших после длительного применения МАБ, после отмены антиандрогенов было отмечено значимое снижение уровня ПСА и даже регрессия первичной опухоли. Этот пародоксальный эффект впервые был зафиксирован при отмене флутамида (Scher H.I., Kelly W.K., 1993; Dupont A., et al., 1993). Позднее подоеный синдром был зарегистрирован для двух нестероидных антиандрогенов — анандрона и касодекса, а также стероидных — мегестрол ацетата и хлорамидинон ацетата, Точный механизм возникновения данного феномена неизвестен, однако считается, что он связан с мутацией андрогенных рецепторов. Показано, что снижение уровня ПСА отмечается у 38%-54% пациентов, причем средняя продолжительность эффекта составляла 2-4 месяца.
До настоящего времени остается открытым вопрос об использовании антиандрогенов как второй линии терапии. Поданным А.М. Гарина (1997), складывается впечатление, что касодекс (бикалутамид) конкурирует с флутамидом и анандроном в практике лечения рака предстательной железы. На ASCO в 1996 году и на XIII конгрессе Европейской ассоциации урологов в Барселоне в 1998 году была представлена серия докладов, посвященных этому препарату. Есть работы, в которых отмечено улучшение от касодекса после прогрессирования на фоне лечения флутамидом (Liebertz С. et аl., 1995). В последнее время проходят испытания высоких доз касодекса — 150 мг, показывающие очень обнадеживающие результаты. Так Fourcade R.O. и Potere М., 1998, показали в сравнительном исследовании на 120 пациентах распространенным раком предстательной железы, что монотерапия касодексом (150 мг) равно эффективна кастрации. На основании полученных данных они считают, что касодекс может считаться альтернативой кастрации при лечении прогрессирующего рака простаты.
Химиотерапия рака предстательной железы. По мнению известных химиотерапевтов, в частности А.М. Гарина (1997), место химиотерапии в системе лечения рака предстательной железы последнее. Лучшим критерием активности химиотерапевтических средств считается падение уровня ПСА, поскольку другие объективные критерии плохо измеряемы и присутствуют лишь у 10% больных. В расчет принимаются качество жизни, субъективный эффект — снятие болей, улучшение общего самочувствие и т.п.
Результаты использования цитостатиков при лечении диссеминированного рака предстательной железы остаются неудовлетворительными. При развитии резистентности к гормонотерапии объективной частичной регрессии опухоли удается добиться менее чем у 10% больных. При изучении эффективности 26 цитостатиков у больных гормонорезистентным раком предстательной железы, положительные результаты составили 8.7% (6.4-9%). Только 6 цитостатиков демонстрируют эффективность 10% и более, среди них винбластин (инфузии), триметрексат, эстрамустин, цисплатин. В ОНЦ РАМН была исследована эффективность отечественного препарата второго поколения соединений платины — циклоплатама. Лечение проведено 26 больным гормонорезистентным раком предстательной железы. Циклоплатам вводился внутривенно капельно на 5% растворе глюкозы из расчета 80-100 мг на м 2 площади тела ежедневно в течение 5 дней. Курс повторялся через 28 дней. Эффективность циклоплатама составила: частичная регрессия — 8.7%, минимальная частичная регрессия ( Активностью в диапазоне 10-20% обладают антрациклины, митоксантрон, эстрамустин, цисплатин, винбластин, фторурацил, циклофосфан. Средняя выживаемость больных, получавших химиотерапию — 40-48 недель. Результаты монохимиотерапии различными препаратами, изучавшимися за последние 10-15 лет, приведены в табл. 62.
Таблица 62. Эффективность монохимиотерапии в лечении диссеминированного рака предстательной железы (Rubben Н. ,1997).
| Химиопрепарат | Кол-во больных |
Общий ответ | Авторы | |
| n | % | |||
| Цисплатин (Cisplatin) |
54 | 24 | 44 | Merrin (1979) |
| 25 | 4 | 16 | Yagoda et al. (1979) | |
| 21 | 4 | 19 | Rossof et al. (1979) | |
| 17 | 0 | — | Qazi et fl. (1983) | |
| 29 | 3 | 10 | Moore et al. (1986) | |
| Циклофосфамид (Cyclophosphamid) |
57 | 8 | 14 | Carter et al. (1975) |
| Доксорубицин (Doxorubin) |
25 | 21 | 84 | Torti et al. (1983) |
| 51 | 7 | 14 | Blum (1975) | |
| 39 | 3 | 8 | Scher et al. (1984) | |
| Этопозид (Etoposide) |
5 | 2 | 40 | Nissen et al. (1984) |
| 36 | 5 | 14 | Walther et al. (1986) | |
| 5-Фторурацил (5-Fluorouracil) |
7 | 1 | 14 | Ansfield et al. (1962) |
| 4 | 1 | 25 | Weiss et al. (1961) | |
| 6 | 3 | 50 | Hall et Good (1962) | |
| Ломустин Lomustine |
19 | 2 | 11 | Carter et al. (1975) |
| Мелфалан Melphalan |
15 | 1 | 7 | Houghton et al. (1977) |
| Митрамицин Mithramycin |
36 | 2 | 6 | Carter et al. (1975) |
| 6 | 2 | 33 | Kofman et al. (1963) | |
| Митомицин-С Mitomycin-C |
4 | 0 | — | Humpherey et al. (1961) |
| 31 | 9 | 29 | Jones et al. (1986) | |
| Митоксантрон Mitoxantrone |
25 | 15 | 60 | Otto et al. (1996) |
| Винбластин Vinblastine |
39 | 8 | 21 | Dexeus et al. (1985) |
| Винкристин Vincristine |
22 | 2 | 9 | Carter et al. (1975) |
| Виндезин Vindesine |
27 | 16 | 59 | Jones et al. (1983) |
Результаты полихимиотерапии гормонорефрактерного рака предстательной железы несколько лучше, однако весьма далеки от желаемых. Различные комбинации цитотоксических препаратов и их эффективность приведены в табл. 63.
Таблица 63. Эффективность полихимиотерапии в лечении гормонорезистентного рака предстательной железы (нерандомизированные исследования).
| Вид лечения | Кол-во больных |
Общий ответ | ПР + ЧР | Авторы | ||
| n | % | n | % | |||
| Циклофосфан + Доксорубицин |
20 | 8 | 40 | 3 | 15 | Izbick et al. (1979) |
| 22 | 11 | 50 | 8 | 32 | Ihde et al. (1980) | |
| 19 | 5 | 26 | 0 | — | Merrin et al.(1976) | |
| 11 | 2 | 18 | 2 | 18 | Lloyd et al. (1976) | |
| 21 | 12 | 57 | 0 | — | Solowayet al. (1979) | |
| 35 | 46 | Fischer et al. (1997) | ||||
| Эстрамустин + 5-фторурацил |
25 | 3 | 12 | 0 | — | Kennealey et al. (1978) |
| Доксорубицин + Платидиам |
21 | 10 | 43 | б.э. | — | Citrin et al. (1982) |
| 17 | 9 | 53 | 9 | 53 | Perloff et al. (1977) | |
| Циклофосфан + Доксорубицин + Платидиам |
17 | 12 | 71 | 7 | 41 | Ihde et al. (1981) |
| Циклофосфан + Платидиам + Преднизон |
22 | 10 | 45 | 0 | — | Berry & MacDonald (1982) |
| Доксорубицин + 5-ФУ + Митомицин С |
62 | 3 | 48 | б.э. | — | Logothetis (1983) |
| 16 | 7 | 44 | 0 | — | Kasimis et al. (1983) | |
| 14 | 9 | 64 | 1 | 7 | Hsu & Babaian (1983) | |
| 5-ФУ + Метотрексат + Винкристин + Мефалон + Преднизон |
84 | 30 | 36 | 3 | 4 | Paulson et al. (1979) |
| 5-ФУ + Циклофосфан |
50 | 34 | 68 | 14 | 28 | Gratf et al. (1990) |
А.М. Гарин с соавт., (1995), предлагают несколько схем полихимиотерапии рака предстательной железы.
IFP — Ифосфамид 2 г в/в, 1-3 дня
Фторурацил 250 мг в/в, 1 -5 дней
Цисплатин 30 мг в/в, 1-5 дней
Интервал между первыми тремя курсами 3-4 недели, далее по 6-8 недель. (Всего 6 курсов).
AC — Адриамицин 40 мг/м 2 в/в, 1-й день
Циклофосфан 200 мг/м 2 внутрь, 3-6 дней
Циклы повторяются каждые 28 дней.
АСВ — Адриамицин 40 мг/м 2 в/в, 1-й день
Циклофосфан 100 мг/м 2 внутрь, с 1-го по 10 день
Кармустин 80 мг/м 2 в/в, 1-й день.
Циклы повторяются каждые 6 недель.
CAF — Циклофосфан 400 мг/м 2 в/в, 1-й и 8-й день
Адриамицин 40 мг/м 2 в/в, 1-й и 8 день
Фторурацил 400 мг/м 2 в/в, 1-й и 8-й день
Циклы повторяются каждые 28 дней.
САМ — Циклофосфан 1 г/м 2 в/в, 1-й день
Адриамицин 30 мг/м 2 в/в, 1-й день
Метотрексат 20 мг/м 2 в/в, 1-й день
Повторный цикл через 4 недели.
РАМ — Фторурацил 600 мг/м 2 в/в, 1, 8, 29 и 36-й день
Адриамицин 30 мг/м 2 в/в, 1-й и 29 день
Митомицин 10 мг/м 2 в/в, 1-й день
Повторные курсы через 3 недели.
Вопросам химиотерапии диссеминированного гормонорефрактерного рака предстательной железы уделялось большое внимание на ASCO в 1996 и 1998 гг. По данным этих симпозиумов, комбинация малых доз преднизолона (5 мг 2 раза в день) и митоксантрона (12 мг/м 2 1 раз в 3 недели) привела к достижению объективной и субъективной ремиссии у 22 из 80 гормонорефрактерных больных. Продолжительность эффекта составила в среднем 43 недели. В контрольной группе, получавшей только преднизолон результаты были достоверно хуже.
Произведена оценка комбинации фторурацила (вводимого длительно 200 мг/м 2 в день в течение 18 недель), эпирубицина (40 мг/м 2 внутривенно) и цисплатина (60 мг/м 2 внутривенно). Препараты назначались 1 раз в 3 недели. Противоопухолевый эффект со снижением ПСА более 50% достигнут в 38% наблюдений. Продолжительность улучшения составила 9 месяцев.
От комбинации этопозида (50 мг внутрь 2 раза в день), цисплатина (70 мг/м 2 ) и эстрамустина (10 мг/кг 2 раза в день) в течение 2 недель с повторением циклов каждые 28 дней, достигнуты ремиссии в 61% случаев. Продолжительность эффекта составляла 6 месяцев. Комбинация Эстрамустина с винбластином обладает эффективностью в 25-54% наблюдений, а эстрамустина с таксотером — в 62%. Сочетание эстрамустина, винбластина, доксорубицина и кетоконазола была эффективной в 75% наблюдений.
Замечен противоопухолевый эффект антитрипаносомного препарата Сурамина (полисульфонат нафтилмочевины). В механизме действия этого агента — связывание рецепторов факторов роста (фибробластного инсулиноподобного и тромбоцитарного). К сожалению, у данного препарата низкий терапевтический индекс. Нейропатии, коагулопатии и надпочечниковая недостаточность встречаются у большинства больных. Вместе с тем, на ASCO последних лет была представлена серия докладов, посвященных сурамину. Считается, что для достижения эффекта должна поддерживаться стабильная концентрация препарата в плазме (285 мг/мл). В этом случае эффективность его составляет 33%, а ее продолжительность — 22 недели. Сурамин комбинируют с полной андрогенной блокадой, при этом 2-х годичная выживаемость больных с метастатическим раком предстательной железы составляет 84% (Dawson N.A. et al.,1995). Комбинация сурамина с гидрокортизоном позволила снизить уровень ПСА более 50% у 43% из 178 больных и привела к частичной регрессии опухоли у 22% из 140 пациентов гормонорезистентным раком предстательной железы (Stemberg С.N.,1998).
Определенные надежды возлагают на ретиноиды (витамин А и его дериваты). Они, как оказалось, тормозят пролиферацию клеток рака предстательной железы in vitro. Уменьшают частоту первичных и метастатических опухолей у крыс, у которых спонтанно развивается рак простаты.
Проявлен интерес к комбинациям альфа-интерферона и ретиноидов. Причем, комбинация активнее употребления каждого из препаратов в режиме монотерапии. Отмечено снижение концентрации сывороточного ПСА у 40 резистентных к гормонам больных.
Совершенно необычные результаты были представлены на ASCO в 1996 г. Damie R. et al. Так ими приведены результаты исследования, в которое вошли 18 больных с прогрессированием рака предстательной железы на фоне гормонотерапии. У всех у них вырос ингибиторный фактор интерферона (IIF) и не продуцировался собственный. Интерферон вводили по пульсовой методике 3 дня в 4 недели, и так в течение двух лет, доза титровалась по концентрации в плазме. Через 12 месяцев полная ремиссия была у 8 из 18 (44%) и частичная у 3 (16.6%, через два года полная ремиссия у 10 из 18 (55%) и у 3 исчезли метастазы в кости, средняя выживаемость — 6 лет.
В ряде пилотных исследований выявлена принципиальная чувствительность рака предстательной железы к таксолу и навельбину. Среди новых препаратов, получающих противоопухолевую оценку при раке предстательной железы — маримостат (ингибитор матрикс металлопротеиназ), финастерид, эпристерид и туростерид (ингибиторы 5-альфа редуктазы), которые уменьшают интрапростатическую концентрацию дигидротестостерона, фенилбутират, тормозящий пролиферацию клеток рака простаты и уменьшающий выработку ПСА. Кроме того проявляется интерес к ингибиторам фактора роста — Со-матостатину и его аналогам, показавшим определенную эффективность в эксперименте на крысах.
Литература
Гарин А.М. 2-я линия эндокринной терапии и химиотерапия генерализованного рака предстательной железы. Материалы Европейской школы онкологов. ОНЦ им. Н.Н. Блохина, М. -1997.
Гарин А.М., Хлебнов А.В. Справочник практической химиотерапии опухолей. М. -1995.
Damie R., Long P. Caglayan S. et al. Prostate carcinoma response to interferon therapy. ASC0 1996, 692.
Dawson N.A. Hormonal therapy for prostate cancer: What you need to know. ASC0 1998, p. 368-372.
Dawson N.A. Steinberg S.M., Figi W.D. et al. A phase 11 trial of leuprolide, flutamide and suramin, in previously untreated metastatic prostate cancer. // ASC0 1995, 617.
Dupont A., Gornez J., Cusan L. et al. Response to flutamide withdrawal in advansed prostate cancer in progression under combination therapy. // J. Urol., 1993, vol.,150, p.908-913.
Fourcade P.O., Chalclain С., Poterre М. An open multicentere randomised stadyto compare the effekt and safety of casodex 150 mg monotherapy with castrathion plus nilutamide in metastatic prostate cancer. Abstr. From the XIII th congress of the EAU, Barselona, 1998. -349.
Isaacs J.T., Lundmo P.I., Berges R. et al. Androgen regulation of programmes cell death of normal and malignant prostatic cells. J. Androl. 1992, Vol. 13, p. 457-464.
Uebertz C., Kelly W.K., Theodoulou M. et al. High dose casodex for prostate cancer: PSA declines in patients with flutamide withdrawal responses. ASC0 1995, 603.
Mahler Ch. Secondare hormonale treatment. First International consultation on prostate cancer. Monaco, 1996, p.305-314.
Fiubben H. Treatment of hormone resistant disease. First International consultation on prostate cancer. Monaco, 1996, p.325-342
Источник medi.ru