Основные причины для проведения МРТ
Для чего проводят МРТ простаты у мужчин и что показывает полученный результат? Так как простата считается наиболее важным органом, входящим в мочеполовую систему мужчин, от её здоровья зависит состояние всего организма. Данная железа выполняет контроль за выработкой веществ, обеспечивающих жизнеспособность сперматозоидов, а также оказывает большое влияние на мочевыделительную функцию.
В связи с большой нагрузкой, возложенной на этот орган, предстательная железа нередко подвергается воздействию неблагоприятных условий и нарушениям в её состоянии, вызванным заболеваниями. Так, рак предстательной железы занимает одно из первых мест в списке болезней с неблагоприятным исходом у мужчин.
Начальные стадии проявляют себя нарушением мочеиспускания с проявлением болезненности и появлением крови в моче.
Затруднения в своевременном обнаружении болезни объясняется отсутствием характерных признаков на первой стадии злокачественных изменений.
Методы, которыми воспользовались на данном этапе, способны принести значительные результаты, когда лечение такого серьёзного заболевания можно ограничить лишь терапией.Проведение МРТ позволяет получить результаты с высокой точностью, причём такой способ может выявить самые различные патологии, в том числе и онкологию в начальной стадии.
В большинстве своём в проведении обследования нуждаются состояния организма при имеющихся подозрениях на злокачественные патологии, а именно в расположении предстательной железы. Процедура совершенно безопасна и безболезненна, а полученные фото отличаются высокой точностью и качеством, благодаря чему можно поставить безошибочный диагноз и назначить правильное лечение.
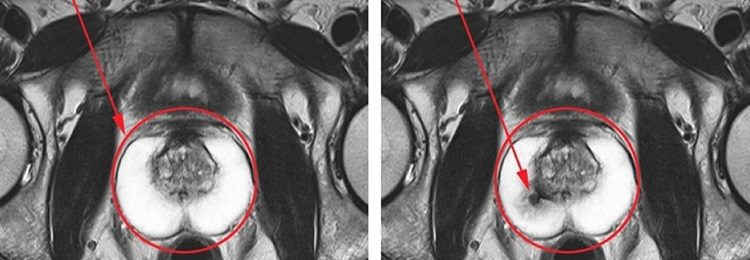
Данный способ позволяет определиться с динамикой злокачественного новообразования, выявить локализацию опухоли и понять, развивается ли она внутри железы или уже выходит за её пределы.

В результате проведения анализов и процедуры МРТ могут быть выявлены следующие состояния:
- определены нарушения функций в органах мочеполовой системы;
- происходит неполное опорожнение мочевого пузыря;
- наблюдаются учащённые позывы к совершению мочеиспускания;
- появление крови в составе мочи.
К проведению исследования с использованием МРТ больного направляют при следующих симптомах:
- разные стадии простатита;
- аденома в предстательной железе, имеющая доброкачественный характер;
- подозрение на рак в железе;
- для проведения оценки состояния регионально расположенных лимфоузлов;
- с целью выявления роста первичного доброкачественного новообразования;
- для выявления возможных метастазов.
Основным показанием к проведению МРТ остаётся злокачественная опухоль в простате. Процедура проводится после предварительного цитологического исследования или после гистологии образцов материала, полученных при биопсии.
При помощи МРТ проводится оценка региональных лимфатических узлов и определяется наличие или отсутствие метастазов в костях таза и в поясничном отделе позвоночного столба. Исследование назначается также для контроля за возможностью развития опухоли в лимфоузлах после проведённого удаления предстательной железы при сохранении возможности рецидива.
Варианты МРТ и их отличия " alt="">
Способы проведения МРТ простаты зависят от модели используемого оборудования, а оно бывает разным.
Классический вариант аппаратуры представляет собой полую цилиндрическую трубу, закрытую со всех сторон. Снаружи цилиндра подключается магнитное поле. Пациент укладывается на стол, двигаемый при управлении извне в центр магнитного поля.
Открытый вариант для исследования представляет собой цилиндр с имеющимися окошками с боковых сторон, где магнитное поле отсутствует.
Виды высокоточной магнитно-резонансной томографии
Современные высокопольные томографы предоставляют возможность проработать полный перечень клинически значимых показателей, увеличив количество вероятных исследований. Достаточный показатель диагностической достоверности дает возможность визуализировать и выполнить осмотр тканевых срезов с толщиной менее 1 мм.
Традиционная
На орган воздействуют высокочастотным магнитным полем.
Волны поглощаются структурами организма с различной интенсивностью.
Образующиеся перепады отображают специализированные датчики, а компьютерное обеспечение визуализирует итоги.
Изображения с патологическими переменами выводятся на пленку в виде цикла снимков.
При выполнении манипуляции очки, съемные протезы, пластиковые карты, мобильные телефоны и украшения требуется убрать.
С контрастом
Магнитно-резонансное исследование простаты проводится при помощи специального компьютерного томографа. В зависимости от особенностей здоровья урологического пациента врач подбирает наиболее подходящий вариант обследования.
На данный момент в медицинских учреждениях проводят следующие виды этой процедуры при раке простаты:
- МРТ простаты с контрастированием – манипуляция, во время которой для улучшения получения визуальной картины вводится безвредное вещество. Парентерально вводимая контрастная жидкость повышает точность дифференциации здоровых и пораженных внутренних органов.
- Исследование, проводимое при помощи специального трансректального датчика (катушки). Вследствие введения в прямую кишку медицинского провода электромагнитное поле находится наиболее близко к простате, что обуславливает высокую точность диагностики. Однако такая форма проведения процедуры сопровождается определенной долей дискомфорта для урологического больного.
- В комплексе с МРТ врач может принять решение о дополнительном проведении спектрограммы, которая позволяет выяснить характер изменений на уровне биохимических процессов, происходящих в тканях пораженной предстательной железы.
Расшифровку результата компьютерного обследования и итоговое врачебное заключение подготавливает врач рентгенолог.

Безопасный и максимально точный метод исследования помогает вовремя выявить самые сложные заболевания, а значит, увеличиваются шансы на выздоровление. Кроме обычного проведения мрт, возможны дополнительные методы, которые еще больше увеличивают точность результата.
1. Процедура с катушкой отличается высокой эффективностью. В прямую кишку вводят провод, который покрыт защитным чехлом из латекса. Он тонкий, гибкий, позволяет фокусировать электромагнитное поле максимально близко к простате. Несмотря на дискомфорт во время проведения МРТ таким образом, результат обследования максимально точный.
2. С введением контрастного вещества, ясно просматриваемого на томографе, через вену, повышается точность результата. МРТ с контрастированием позволяет визуально разделить больные и здоровые ткани.
3. Одновременно с исследованием, с помощью томографа иногда назначается проведение спектрограммы. Таким образом, становится возможным определить точное химическое строение тканей предстательной железы.
Подобные методы проводятся отдельно или в комплексе для достижения максимального эффекта. Магнитно резонансный томограф позволяет своевременно выявить рак, что дает реальный шанс без операции излечиться от недуга.
Еще один вид МРТ — прицельное исследование простаты. Его проводят на сверхвысокопольном оборудовании с использованием брюшной катушки. Такой метод может стать альтернативой биопсии предстательной железы.
Диффузно-взвешенная МРТ диагностика — метод исследования в результате которого появляются новые возможности в выявлении рака простаты с помощью визуализирования молекулярной диффузии. Оценить характер диффузии можно за счет влияния на скорость взаимообмена случайных движений молекул воды в тканях и органах.
Медленно протекающий процесс диффузии говорит о наличии опухолевого образования. В клетках злокачественной опухоли с низким коэффициентом диффузии содержится очень мало воды, следовательно они от здоровых клеток отличаются, выделяясь на их фоне.
На МРТ рак предстательной железы хорошо визуализируется, увеличивая диагностическую возможность данного метода.
Классическое исследование
Во время выполнения МРТ исследования пациента укладывают на подвижный стол, который вкатывают внутрь конструкции цилиндрической формы, которая окружена магнитами. Если есть необходимость, пациенты фиксируют в правильном положении с помощью ремней или подушек. Крайне важно во время исследования лежать неподвижно, именно этот фактор гарантирует точность результатов, в ином случае возможна ошибка.
МРТ простаты с контрастированием
В кровь внутривенно вводят контрастное вещество, которое на экране аппарата хорошо различается. Это позволяет определить, где пораженные, а где здоровые ткани. Только специалист принимает решение о необходимости исследования методом МРТ с контрастом. Обследование назначают в основном при подозрении на онкологию предстательной железы.
Контрастное вещество вводят в вену пациенты непосредственно перед процедурой. В остальном процедуру проводят так же, как и при традиционном методе.
МРТ с эндоректальной катушкой
- Перед исследование не рекомендуют употреблять кисломолочные продукты, хлебобулочные изделия и продукты с грубой клетчаткой.
- За сутки выпивают уголь активированный из расчета на 10 килограммов веса две таблетки.
- Пищу прекращают принимать за пять часов до процедуры.
- За час до процедуры рекомендуют принять таблетку Но-шпы.
Перед тем, как идти на процедуру, пациент оставляет за пределами кабинета, где будет проводиться исследование, банковскую карту, украшения, ключи или другие металлические предметы. Одежда так же должна быть без металлических пуговиц, клепок и других украшений. Как правило, пациента переодевают в специальную одежду.
Пациент располагается на подвижном столе. Его положение фиксируют подушками или ремнями. Мужчина во время сканирования должен быть полностью неподвижен. От этого зависит точность результатов исследования. Если есть необходимость проведения МР-спектроскопии, доктор проводит соответствующую процедуру.
Эндоректальную катушку, с надетым на нее чехлом, вводят в анальное отверстие, смазав лубрикантом. После проведения подготовительных процедур, пациента помещают внутрь аппарата. После исследования катушку вынимают, а больного просят обождать до определения качества изображения.
Врач-радиолог изучает результаты исследования, в ходе которого он оценивает состояние простаты, капсулы, семенных пузырьков, окружающих тканей и регионарных лимфоузлов. Расшифровка позволяет лечащему врачу исключить или подтвердить патологии, а так же получить все сведения о состоянии предстательной железы.
Мультипараматическая МРТ
Метод объединяет все виды МРТ простаты. Преимущество диагностики – обнаружение злокачественной опухоли на самой ранней стадии.
Многомерная и многоплановая реконструкция изображения позволяет полностью исключить возможность ошибки. Врач оценивает состояние органа под разным углом обзора и по разным параметрам.
Часто методику совмещают с биопсией, что позволяет обнаружить самые агрессивные области. Определив место локализации опухоли, врач выполняет точечную биопсию. При других проведения биопсии множественные проколы осуществляют наугад в разные точки.
Мульти-параметрическая МРТ позволяет точно определить степень распространения онкологии. Это дает возможность определить стадию и риски развития патологии, а соответственно назначить эффективную терапию.
Удаление яичек у мужчин: фото, операция, последствия
Устаревшим термином «аденома простаты» или, по-новому, «доброкачественная гиперплазия предстательной железы» обозначается разрастание клеток железистой ткани органа под названием «простата». Такой аномальный рост тканей хорошо виден на фото УЗИ.
ДГПЖ обычно начинается, когда мужчине исполняется 30 лет.
Болезнь развивается неспешно и обычно вызывает признаки аденомы простаты мужчин на 50 году жизни или позже.

Причина патологии пока не ясна. Известно лишь, что она связана с концентрацией мужских половых гормонов, которая снижается по мере старения.
- Величина простаты не всегда связана с большим дискомфортом.
- У более старых людей симптомы ДГПЖ часто проявляются более явно, чем у молодых.
- Аденома простаты — опухоль хотя и ухудшающая качество жизни, но не злокачественная.
- Некоторые лекарственные препараты могут усилить симптомы аденомы простаты. К ним относятся некоторые антигистаминные, противоотечные и назальные спреи.
‘); > d. write(»); var e = d.
createElement(‘script’); e. type = «text/javascript»; e.
src = «//tt. ttarget/s/tt3.
js»; e. async = true; e.
onload = e. readystatechange = function () < if (.
e. readyState || e.
readyState == «loaded» || e. readyState == «complete») < e.
onload = e. readystatechange = null; TT.
ttarget/s/tt3. ws’); s.

createBlock(b); >; >; d. getElementsByTagName(«head»)[0].
Как проходит МРТ-диагностика предстательной железы?
Процедура сканирования предстательной железы проводится в несколько этапов:
- Подготовка пациента к МРТ и предварительная консультация у специалиста.
- Само сканирование. После введения контрастного вещества и эндоректального датчика в специальном чехле, смазанном лубрикантом, мужчина ложится на специальную кушетку, фиксируется ремнями. Затем подвижная кушетка въезжает в трубу томографа.
- Завершение обследования. Кушетка выезжает из томографа. Пациента освобождают от ремней, извлекают датчик из прямой кишки.
- Обработка полученных данных. Обычно врач практически сразу сможет распечатать сделанные снимки и записать всю информацию на электронный носитель. Но для расшифровки необходимо немного подождать.
После процедуры контрастное вещество без каких-либо дополнительно принятых мер выводится из организма пациента естественным путём. А сам человек может продолжать вести свой привычный образ жизни и отправляться домой.
Наблюдение за пациентом при проведении антиандрогенной терапии и после лучевой терапии с помощью МРТ является проблемным. Длительно проводимая андрогенная блокада и облучение ведут к характерным гистологическим изменениям. Как в центральной, так и в периферической зонах не удается найти разграничений между опухолевой тканью и регрессивно-фибротическиии изменениями железистой ткани.
Нельзя с уверенностью ответить на вопрос: позволяет ли МРТ отличить активный рост опухоли от оставшейся опухоли. В дальнейшем проблемой в наблюдении за пациентом с раком простаты становится определение рецидива опухоли и метастазирования.
Клиническим подозрением на рецидив опухоли является повышение уровня ПСА через определенный период после относительно благоприятного течения. Причины повышения ПСА многообразны: локальный рецидив после радикальной простатэктомии или облучения, активный рост опухоли, наличие лимфогенных или появление костных метастазов.

Рак предстательной железы – это тяжелое заболевание, которое часто встречается у мужчин пожилого возраста. В редких случаях подобная онкология может быть обнаружена и у молодого мужчины.
При отсутствии необходимого лечения или активном процессе распространения опухоли, новообразования могут появляться в других органах – в данном случае речь идет о метастазировании. Чаще всего метастазы при этом наблюдаются в легких, в печени и мочевом пузыре.
Виды метастазирования
Выделяют несколько видов метастазирования:
- Местное — поражение раковыми клетками соседствующих тканей и органов.
- Интравазация – поражение раковыми клетками лимфоузлов и кровотока.
- Задержанное – «приостановка» распространения раковых клеток и их скопление в сосудистых капиллярах.
- Ангиогенез – поражение небольшим количеством раковых клеток кровеносных сосудов.
- Циркуляция – поражение раковыми клетками соседствующих органов и тканей через лимфоузлы.
- Пролиферация – поражение соседствующих органов и тканей раковыми клетками микроскопического размера.
Метастазы распространяются на другие органы и ткани через кровь.
Наличие метастаз в других органах при раке предстательной железы является основанием для диагностики третьей степени заболевания.
При этом после того, как онкология поразит соседние органы и ткани, она распространяется на костную систему организма и печень. В мягких органах метастазы образуются после практически полного разрушения крупных сосудов.
| Биопсия простаты: виды, противопоказания, осложнения, результат |
| Что такое рак простаты: симптомы и признаки болезни |
| Как проводится гормонотерапия при раке простаты у мужчин |
| Лечение рака простаты народными средствами в домашних условиях |
Удаление яичек у мужчин: фото, операция, последствия
Средняя чувствительность МРТ при выявлении РПЖ (в первую очередь, микроскопических очагов) не позволяет использовать этот метод для исключения неопластического процесса.
При биохимическом рецидиве рака после радикальной простатэктомии МРТ позволяет с 97-100% точностью выявить локальный рецидив опухоли или метастазы в регионарные лимфатические узлы.
Точность МРТ при выявлении очагов неопластического поражения предстательной железы составляет 50-90%. Чувствительность МРТ в локализации РПЖ составляет около 70-80%, при этом микроскопические очаги рака нельзя выявить с помощью МРТ.
Гиперинтенсивность на Т2-взвешенных изображениях муцинозной аденокарциномы предстательной железы затрудняет диагностику и приводит к ложноотрицательным результатам МРТ.
Клиническая информация (уровень ПСА, ранее проведённое лечение), знание анатомии предстательной железы, использование эндоректального датчика, динамического контрастирования и спектроскопии позволяют приблизить точность выявления очагов рака с помощью МРТ к 90-95% (в большей степени повышается специфичность).
Чувствительность МРТ в отношении эксграпростатической экстензии находится в пределах 43-87%, что, в первую очередь, связано с невозможностью визуализации микроскопического прорастания капсулы предстательной железы.
Чувствительность выявления экстензии глубиной менее 1 мм при эндоректалыюй МРТ составляет всего 14%, тогда как при прорастании опухоли за пределы железы более чем на 1 мм показатель возрастает до 71%.
Источник prostatitnik.ru
Ультразвуковые исследования в диагностике рака предстательной железы
Трансректальное ультразвуковое сканирование обладает явным преимуществом по сравнению с абдоминальным сканированием ввиду близкого соприкосновения датчика с предстательной железой.
Сканирование в сагиттальной и фронтальной проекциях позволяет наиболее полно обследовать предстательную железу.
Появившиеся в последнее время технические возможности (цветная допплерография и трехмерное сканирование с использованием контрастных средств) значительно повысили диагностические возможности данного вида исследования.
Случаи рака предстательной железы выглядят гипоэхогенными зонами при трансректальном ультразвуковом исследовании (ТРУЗИ), хотя они могут быть и изоэхогенными, а иногда и гиперэхогенными. Наличие других изменений в предстательной железе в виде асимметрии размеров, формы и эхогенности, нечеткое разделение между центральной и периферическими зонами, деформация и деструкция капсулы также позволяют заподозрить наличие рака при выполнении ТРУЗИ.
Деформация и неправильная форма капсулы в участках, прилегающих к гипоэхогенному узду предстательной железы, позволяют предположить экстрапростатическое распространение опухоли. Трансректальное ультразвуковое исследование можно использовать для определения инвазии в семенные пузырьки. Однако ТРУЗИ не может считаться достоверным методом в оценке стадии процесса. Чувствительность этого метода определена в пределах 71-92%, специфичность — 49-79%. По мнению R.L. Waterhouse, M.I. Resnick (1998), трансректальное ультразвуковое исследование имеет прогностическое значение в 30% случаев.
Гораздо большее, хотя и неоднозначное, значение в определении стадии имеют компьютерная и магнитно-резонансная томография.
Мнения ученых о ценности клинического применения компьютерной томографии (КТ) для определения распространенности рака предстательной железы диаметрально противоположны. По мнению С.К. Ноn и соавт. (1998), G.J. Jager и соавт. (2000), компьютерная томография имеет незначительное значение или вовсе не играет роли при оценке локального процесса.
Она не позволяет отличить злокачественный процесс от доброкачественного и достоверно определить наличие экстракапсулярной инвазии или инфильтрации семенных пузырьков. В стадиях Т3-Т4 КТ демонстрирует увеличение железы, распространение инфильтрата на окружающие органы. В стадиях Т1-Т2 возможности ограничены из-за практически одинаковой плотности тканей.
Точность компьютерной томографии в стадировании рака предстательной железы невелика и составляет менее 60%, но ее ценность, по мнению R.C. Flangian и соавт. (1996), возрастает при оценке вовлечения в процесс семенных пузырьков до 70%.
Итак, клиническое применение компьютерной томографии в определении стадии рака простаты в целом не оправдано. КТ играет минимальную роль в опенке локальной формы болезни, она не демонстрирует внутреннюю архитектонику железы, не способна различить рак и доброкачественный процесс в простате и надежно идентифицировать экстракапсулярное распространение или инвазию в семенные пузырьки. Компьютерная томография не обеспечивает дополнительной информацией для сталирования локальной формы болезни в большей степени, чем пальцевое ректальное исследование.
Из-за низкого определения позитивных лимфатических узлов ценность применения КТ для этих целей также незначительна. Большинство лимфатических метастазов микроскопические, и они не увеличивают или не искажают лимфатические узлы.
Достоверно доказано, что есть группы пациентов, для которых риск поражения лимфатических узлов может быть выше: Простатспецифический антиген (ПСА) от 20 до 30 нг/мл или низкодифференцированная опухоль (сумма Gleason >7 при биопсии) определяет риск макроскопических изменений, что оправдывает проведение КТ. Необходимо обратить внимание на то, что при наличии увеличенного лимфатического узла, выявленного на компьютерной томографии, необходимо подтвердить злокачественный процесс в ткани самой железы (рис. 3.7).

Рис. 3.7. Диссеминированный рак предстательной железы. Выход за пределы капсулы железы, инвазия в сосудисто-нервный пучок. Поражение лимфатических узлов по ходу подвздошных сосудов
Кроме того, внедрение в клиническую практику современных методов диагностики и скрининговых программ позволяет выявлять ранние стадии рака, поэтому метастазы в лимфатические узлы обнаруживаются гораздо реже.
13 настоящее время только у 2-3% пациентов, перенесших радикальную простатэктомию (РПЭ) по поводу локального рака, диагностируются метастазы в лимфатические узлы на основании послеоперационного гистологического исследования. Низкая частота позитивных тазовых лимфатических узлов до РПЭ побуждает хирургов отказаться от лимфаденэктомии во многих случаях.
Широко известны номограммы, которые позволяют прогнозировать риск наличия метастазов, и если риск наличия метастазов меньше 2%, лимфаденэктомия может не выполняться. Эти номограммы включают следующие параметры: клиническую стадию, гистологическую степень дифференцировки и уровень ПСА.
МРТ при стадировании рака простаты
Магнитно-резонансная томография при раке предстательной железы (РПЖ) обладает рядом преимуществ. Различная интенсивность сигнала от мягких тканей таза позволяет дифференцировать его различные структуры, использование T1 и Т2-взвешенных изображений взаимно дополняет друг друга. Магнитно-резонансная томография (МРТ) сканеры способны к созданию изображений в поперечной, сагиттальной и коронарной проекциях, а применение эндоректального датчика улучшает визуализацию интра- и ретропростатической анатомии.
При использовании только Т1-взвешенных изображений невозможно оценить внутреннюю архитектонику простаты, хотя ясно видны границы между простатой, семенными пузырьками и окружающим жиром, в то время как Т2-взвешенные изображения способны продемонстрировать интрапростатическую анатомию. В норме периферическая зона предстательной железы возвращает сигналы высокой интенсивности, в то время как рак простаты отображается сигналами относительно низкой интенсивности (рис. 3.8).

Рис. 3.8. РПЖ. T3NXM0. Аксиальные Т2-ВИ предстательной железы. Размеры железы не увеличены. Зональная дифференциация снижена, периферическая зона сохранена фрагментарно. Периферическая зона в задних и заднебоковых отделах слева замешена зоной диффузного понижения интенсивности сигнала на Т2-ВИ с инвазией капсулы железы на большом протяжении и выраженным распространением на прилежащую парапростатическую клетчатку
N. Bloch и соавт. (2003), оценивая эффективность различных типов изображений МРТ в стадировании пациентов перед радикальной простатэктомией, показали точность стадирования при Т1-взвешенных изображениях у 76% пациентов, при Т2-взвешенных — у 84%, а при их комбинации — у 92%.
Однако большинство доброкачественных заболеваний простаты, таких как доброкачественная гиперплазия предстательной железы (ДГПЖ), простатит, особенно калькулезный, также отображаются сигналами низкой интенсивности. Более того, МРТ не продемонстрировала большую точность стадирования рака по сравнению с ТРУЗИ. Вместе с тем дополнение поперечных (аксиальных) сканов коронарным и сагиттальным сканированием позволяет увеличить точность стадирования РПЖ с 61 до 83%.
Наличие на томограммах экстракапсулярного распространения рака простаты можно предположить, если есть очевидная асимметрия, нерегулярность или «бреши» в перипростатическом жире, который в отличие от простаты посылает сигналы низкой интенсивности.
Таким образом, при магнитно-резонансной томографии существуют проблемы относительно диагностики экстракапсулярного распространения. В действительности у предстательной железы нет истинной эпидермальной капсулы и инфильтрация тонкой фибромускулярной капсулы указывает на распространение процесса за пределы железы. МРТ не может идентифицировать микроскопическую пенетрацию за границу простаты и поэтому ограничена в обнаружении прорастания рака.
Опухоль может быть описана как Т2, то есть без пенетрации капсулы, даже если существует широкая область контакта между ней и краем железы, пока края железы не деформированы, так же, как и опухоль, где широкая область контакта сочетается с капсулой и гладкое капсульное выпячивание классифицируется как опухоль стадии Т2.
Нерегулярная выпуклость края простаты, асимметрия нервно-сосудистых пучков (связок) или исчезновение ретропростатического угла указывают на стадию Т3. При стадии Т3 потеря симметрии между нервно-сосудистыми пучками связана с прямым экстрапростатическим распространением рака с периневральными и периваскулярными компонентами.
Точно так же потеря нормального слоя жира между задней поверхностью простаты и передней поверхностью прямой кишки указывает на распространение процесса в перипростатический жир. Когда определяются асимметрия сосудисто-нервных пучков и облитерация ретропростатического угла, стадия Т3 может быть диагностирована с высокой степенью вероятности (рис. 3.9).

Рис. 3.9. РПЖ стадии T3NXM0. Аксиальные Т2-ВИ изображения предстательной железы. Размеры железы умеренно увеличены. Зональная дифференциация снижена, периферическая зона сохранена незначительно, фрагментарно, в правых боковых и левых заднебоковых отделах. В правых заднебоковых отделах определяется протяженная зона понижения интенсивности сигнала с выраженной на большом протяжении инвазией капсулы и инфильтрацией прилежащей парапростатической клетчатки. В левых боковых и центральных отделах железы выявляется диффузная зона снижения сигнала с умеренно выраженной инвазией капсулы. Умеренно выражен отек парапростатической клетчатки по левым боковым отделам железы
R. Palasak и соавт. (2003) выполнили 66 пациентам МРТ перед радикальной простатэктомией и сравнили ее результаты с послеоперационными гистологическими заключениями. Точность стадирования составила 81,8%. В то же время S.A. Brassell и соавт. (2003) показали корреляцию МРТ-стадирования с патологической стадией только у 43% пациентов.
Вовлечение семенных пузырьков определяется присутствием фокуса или диффузных областей низкой плотности вокруг или в пределах семенных пузырьков на Т2-изображениях (рис. 3.10).

Рис. 3.10. РПЖ в стадии T3NXM0. Саггиттальные Т2-ВИ изображения предстательной железы. Размеры железы увеличены за счет гиперплазии центральной зоны. Периферическая зона истончена, с неравномерной инвазией, более выраженной в задневерхних отделах, с инфильтрацией парапапростатической клетчатки и медиальных отделов семенных пузырьков. МР картина опухолевого поражения периферической зоны предстательной железы на фоне гипереплазии ее центральной зоны с протяженной инвазией капсулы и инфильтрацией парапростатической клетчатки и семенных пузырьков
Инвазия в семенные пузырьки указывает на сталию Т3 болезни, которая обычно рассматривается как неоперабельная. Однако существует ряд других заболеваний, которые могут быть причинами подобных проявлений, например неспецифический фиброз, геморрагии после биопсии, амилоидоз, склероз после лучевой терапии.
Магнитно-резонансной томография имеет признаки вовлечения семенных пузырьков хотя и чувствительны, но относительно неспецифичны. Проблема геморрагии после биопсии — также фактор, который влияет на точность МРТ в обнаружении вовлечения в патологический процесс семенных пузырьков.
Геморрагии после биопсии и рак простаты одинаково могут проявляться сигналами низкой интенсивности на Т2-изображениях. Однако они могут дифференцироваться на Т1-изображениях, где постбиопсийные геморрагии проявляются сигналом яркой интенсивности, а опухоль остается гипоинтенсивной.
МРТ при локализованных формах рака простаты включает оценку состояния тазовых и внутрибрюшинных лимфатических узлов (рис. 3.11).

Рис. 3.11. Метастазы в лимфатические узлы
Исследование информативно, когда критериями метастатического поражения лимфатических узлов являются их размеры. Так же как и КТ, магнитно-резонансная томография не способна обнаружить микрометастазы в лимфатические узлы.
Радионуклидное сканирование костей
Осевой скелет — предпочтительное место для метастазирования рака простаты. Наиболее чувствительный и широко используемый метод обнаружения костных метастазов — сцинтиграфия костей с 99т-технецием. Ложноотрицательные результаты встречаются менее чем у 1 % пациентов (из-за присутствия широко распространенных симметричных метастазов).
В то же время ложноположительные результаты относительно часты, поскольку сканирование диагностирует не только метастазы, но и дегенеративные изменения, предшествующую травму, излеченные переломы, нарушение обмена веществ и воспалительно-инфекционные повреждения скелета.
Результат положительного сканирования костей может сопровождаться подтверждающими рентгеновскими снимками, хотя в половине случаев изменения костного скелета появляются прежде, чем повреждение может быть обнаружено простыми рентгенограммами.
МРТ может быть полезно в дифференциальном диагнозе подозрительных областей, выявленных при сканировании, когда они не проявляются на простых рентгенограммах, особенно в осевом скелете. Еще 10-15 лет назад радионуклидное сканирование костей скелета выполнялось часто, так как метастатическое поражение костей скелета наблюдаюсь у 30-35% пациентов с первично выявленным раком простаты. Сегодня эта цифра в США составляет менее 5%.
F.M. Chybowski и соавт. (1991) впервые поставили под сомнение необходимость радионуклидного сканирования всем пациентам с впервые выявленным раком простаты. Отрицательные результаты сканирования костей были получены у 99,7% больных с уровнем ПСА менее 20 нг/мл. В 1995 г. группа экспертов Американской ассоциации урологов заявила, что сканирование костей «больше не является обязательным» для пациентов с впервые диагностированным раком простаты, уровнем простатспецифического антигена менее 10 нг/мл и отсутствием «костных» симптомов.
Итак, радионуклидное сканирование костей скелета рекомендуется:
• пациентам с клиническими стадиями Т1 и Т2 при уровне ПСА >10 нг/мл и сумме баллов по шкале Глисона >8;
• пациентам с клиническими стадиями Т3 и Т4;
• пациентам с «костными» симптомами.
Лимфаденэктомия
С началом эры ПСА у большего количества мужчин рак простаты стал выявляться в локализованной форме, которая вылечивается с помощью радикальной простатэктомии.
Рак предстательной железы склонен к инвазии и метастазированию, поэтому так остро стоит вопрос о ранней диагностике и радикальном лечении больных с локализованными формами РПЖ. Точное знание распространенности заболевания крайне необходимо до начала лечения.
Диагностика лимфогенных метастазов в малом тазе сложна, и имеется большая вероятность ошибки (50-60%) даже при применении всех современных методов диагностики. Ультразвуковое исследование, рентгеновская компьютерная томография, магнитно-резонансная томография могут выявить метастазы, когда размер лимфатических узлов превышает 2 см в диаметре, однако эти методы диагностики не позволяют обнаружить мелкие и микроскопические метастазы.
Одним из существенных недостатков этих методов является отсутствие возможности получения биопсии лимфатического узла для морфологической верификации диагноза, которая является истинно объективным критерием оценки состояния регионарных лимфатических узлов.
Самую надежную информацию можно получить после тазовой лимфаденэктомии с последующим гистологическим исследованием лимфатических узлов методом ступенчатых срезов.
В урологии наибольшее распространение при определении стадии рака предстательной железы получила лапароскопическая тазовая лимфаденэктомия (ЛТЛ). D. Fahlenhamp и соавт. (1997) произвели билатеральную ЛТЛ у 200 пациентов РПЖ с клиническими стадиями Т1-Т3 и уровнем простатспецифического антигена в среднем 44 нг/мл. Удалялось в среднем 11 лимфоузлов. Метастазы в лимфатических узлах были обнаружены у 44 (22%) пациентов. Незначительные осложнения были у 15 (7,5%), серьезные возникли у 8 больных и потребовали открытой ревизии.
Таким образом, с учетом вышеизложенного можно заключить, что ЛТЛ позволяет обнаружить метастазы в тазовых лимфатических узлах, которые не выявлены традиционными методами исследования; определить целесообразность радикального хирургического лечения; обоснованно применить методы системного воздействия на опухолевый процесс.
Искусственные нейронные сети
В урологической практике постоянно присутствует необходимость клинического прогнозирования течения болезни индивидуально для каждого пациента. Прогнозирование может касаться распределения пациентов по группам риска, постановки диагноза, прогнозирования стадии рака, результатов лечения, вероятности рецидива болезни и т.д.
Традиционно прогнозирование основано на статистических классификационных моделях, предполагающих в лучшем случае установление статистических взаимоотношений, которые позволяют определить только ограниченные типы относительно простых нелинейных межпеременных взаимосвязей и в худшем случае допускают линейные отношения среди всех переменных.
Поскольку клинические данные характеризуются большим разбросом, им присущи нелинейные межпеременные взаимосвязи, поэтому статистические модели часто теряют желательную точность, когда используются в клинической урологической практике.
Применение искусственного интеллекта при раке предстательной железы преследует решение следующих задач:
• скрининг рака предстательной железы;
• диагностику рака простаты;
• стадирование опухолевого процесса;
• прогнозирование развития опухоли;
• прогнозирование результатов лечения.
В 1994 г. Snow и соавт. впервые сообщили об использовании ретроспективного программирования (обратного распространения) искусственной нейронной сети (ИНС), для предсказания вероятности положительной биопсии простаты при скрининге населения. Они развили ИНС, которая могла предсказывать вероятность наличия рака простаты при биопсии с чувствительностью 70%, специфичностью 92% и точностью 87%. Эта сеть, которая использовала доклинические переменные (возраст, общий ПСА, результаты ТРУЗИ и пальцевое ректальное исследование (ПРИ), была сформирована более чем на 1500 случаях и прошла проверку на новых 200 контрольных случаях.
Считается, что наиболее важными показателями для анализа с помощью искусственного интеллекта являются свободный ПСА (или же процент его отношения к общему ПСА) и данные ТРУЗИ. Выявлено, что диагностика с помощью искусственных нейросетей позволяет достичь точности от 70 до 85%. Успешно применена нейросетевая технология для формирования групп пациентов с высокой и низкой вероятностью распространения злокачественного процесса в регионарные лимфатические узлы.
Тестирование системы во многих медицинских центрах определило точность прогноза в 98-99% случаев в группе с низкой вероятностью лимфогенного метастазирования (около 57% всех пациентов) и точность прогноза, равную 25% при чувствительности 95% в группе с высокой вероятностью лимфогенного метастазирования.
Нейронные сети, должным образом обученные, демонстрируют превосходящую прогностическую точность по отношению к регрессионному анализу со множественными переменными.
Большинство существующих исследований, где используются ИНС при раке простаты, были выполнены ретроспективно при изучении базы данных. Чтобы должным образом оценить ИНС, необходимы большие проспективные исследования.
При дальнейшем развитии онкологии, выявлении новых опухолевых маркеров искусственные нейросети будут играть все большую роль в раннем выявлении, диагностике, стадировании и лечении рака предстательной железы. Более того, эффективность использования такого мощного инструмента повышается в тех случаях, когда в распоряжении врача имеется множество изменяющихся параметров, а их взаимосвязь друг с другом недостаточно известна.
В урологической клинике Российской медицинской академии последипломного образования на базе клинической больницы им. С.П. Боткина сотрудником кафедры И.В. Лукьяновым (2001) впервые были применены элементы искусственного интеллекта для оптимизации диагностической и лечебной тактики у пациентов, страдающих доброкачественной гиперплазией простаты.
В заключение приводим алгоритм диагностики при подозрении на рак предстательной железы, предложенной R.S. Kirby (2003) и Б.П. Матвеевым (2003).
Алгоритм диагностики при подозрении на рак предстательной железы
Источник medbe.ru
Рак предстательной железы (РПЖ) – актуальная проблема современной онкологии, т.к. заболеваемость растет, а своевременное установление диагноза часто затруднительно из-за низкой специфичности основных неинвазивных исследований.
Как известно, существуют три базовых метода, которые применяют в качестве скрининга при РПЖ:
- Пальцевое ректальное исследование – ПРИ.
- Определение в сыворотке уровня PSA (простатоспецифического антигена).
- Трансректальное ультразвуковое исследование (ТРУЗИ).
Точность диагностики при помощи этих методов не превышает 33%.
«Золотым стандартом» постановки диагноза остается биопсия органа. Но это инвазивное вмешательство, проведение его сопряжено с определенными трудностями и иногда несогласием пациента, к тому же эта процедура также не всегда позволяет верифицировать опухоль с первого раза.

Поэтому так актуально применение других неинвазивных способов диагностики, превышающих специфичность традиционных обследований. Огромную роль здесь играет МРТ.
Суть метода МРТ
Магнитно-резонансная томография на сегодняшний день является, пожалуй, самым точным методом визуализации. Преимущества: исследование безболезненно, безопасно для здоровья, намного информативнее других неинвазивных вариантов.
Принцип – воздействие магнитного поля на клетки, а точнее – на атомы водорода в них. Известно, что организм человека на 80% состоит из воды, и водород, соответственно, присутствуют во всех структурах. Это простейший атом, состоящий из одного протона и электрона. Протон находится в постоянном вращении и имеет собственный магнитный момент.
Во время диагностической процедуры человек помещается в сильное постоянное магнитное поле. Одновременно на него воздействуют переменным электромагнитным излучением. Под влиянием радиочастотного сигнала атомы водорода выстраиваются особым образом (намагничиваются), а при прекращении воздействия – возвращаются в исходное состояние (релаксация). Этот момент возврата сопровождается высвобождением энергии, которую фиксирует аппарат МРТ, получая четкое анатомическое изображение.
Время, за которое происходит релаксация, изменяется в зависимости от вида ткани и наличия патологии в ней. Выделяют два варианта:
- T1- продольная релаксация.
- T2 – поперечная релаксация.
Соответственно получают T1 и T2-взвешенные изображения ( T1 ВИ, T2 ВИ).
Снимки получаемых сигналов проводятся послойно и из нескольких проекций, в результате формируется трехмерная картина исследуемой области. На T1ВИ хорошо видны анатомические структуры и окружающие ткани, T2ВИ – лучше просматривают патологические изменения в самом органе.
МРТ не несет в себе вредного излучения, но противопоказана при наличии в организме электронных устройств и имплантатов из намагничивающихся сплавов.
Роль МРТ при диагностике РПЖ
Магнитно-резонансная томография не является рутинным методом. Назначение ее для первичной диагностики рака простаты неоправданно. Проводят его:
- При сомнительных данных основных методов (пальцевого ректального исследования, ТРУЗИ, повышенном уровне ПСА).
- При сохраняющемся подозрении на РПЖ и отрицательных результатах биопсии.
- После подтвержденной гистологической структуры – для уточнения стадии новообразования.
- Обязательна при выявлении очагов > 0,5 см и суммой баллов по Глисону>7, а также при опухолях более 1 см и любым индексом злокачественности.
- Иногда – для определения места забора ткани на анализ (прицельная биопсия с использованием технологии совмещения данных МРТ и УЗИ –Fusion Biopsy). Перед проведением брахитерапии или дистанционной лучевой терапии – для получения 3D мишени.
- МРТ при раке простаты используется и как метод контроля и динамического наблюдения после лечения.
Возможности
Оценить состояние предстательной железы.
Уточнить размеры и распространение опухоли, диагностированной при помощи УЗИ.
Увидеть рак в начальной стадии в передних отделах периферической зоны, которые недоступны ТРУЗИ.
Установление прорастания капсулы железы.
Вовлечения в процесс уретры, мочевого пузыря, окружающей клетчатки, семенных пузырьков.
Диагностика поражения лимфатических узлов.
Определение метастатических очагов в костях таза, крестца.
Противопоказания к МРТ
Электронные и различные намагничивающиеся имплантаты в организме являются противопоказанием к проведению МРТ. Они могут выйти из строя, сместиться, вызвать ожог или создать помехи при получении данных.
- Имплантированный кардиостимулятор.
- Кохлеарный имплантат.
- Инсулиновая помпа.
- Металлические клипсы на сосудах.
- Тяжелое состояние.
При наличии таких обстоятельств пациенту рекомендуется проведение КТ малого таза с контрастным усилением.
Относительные противопоказания в большинстве случаев могут быть сняты, они рассматриваются индивидуально. Современные импланты, как правило, не обладают ферромагнитными свойствами и совместимы с МРТ исследованиями.
- Эндопротезы суставов.
- Зубные импланты и протезы.
- Стенты в сосудах.
- Искусственные клапаны в сердце.
- Послеоперационные скобки.
- Кава фильтры.
- Клаустрофобия.
- Вес больше 130 кг.
В последних двух случаях обследование можно провести в томографе открытого типа.
Подготовка
Если планируется МРТ простаты с использованием эндоректального датчика, за 12 часов до процедуры не рекомендуется употреблять тяжелую пищу. Накануне обследования кишечник очищается с помощью клизмы.
Непосредственно перед процедурой необходимо снять с себя все металлические украшения, съемные зубные протезы, одежду с металлическими застежками.
Пациент укладывается на выдвижной стол. В уши вставляются наушники или беруши, так как оборудование во время работы производит громкий шум.
В зависимости от применяемой методики помещается на низ живота или в прямую кишку дополнительная катушка. Стол задвигается внутрь камеры.
Само исследование занимает 20-30 минут. Необходимо максимально сохранять неподвижность. Для связи с лаборантом в камере есть кнопка или микрофон.
Стандартное обследование
Это получение T1 и T2 взвешенных протонных изображений в различных плоскостях. В большинстве случаев дает полную информацию о характере, локализации и распространенности патологического процесса. Для усиления магнитного поля в области малого таза используются дополнительные индукционные катушки:
С контрастированием
Применение контрастного вещества (Гадовист) усиливает разницу между нормальной и патологической тканью.
С динамическим контрастированием
Исследует скорость и характер прохождение контрастного вещества через орган после его внутривенного введения. В злокачественных опухолях происходит ускоренное поглощение и более быстрое «вымывание» по сравнению с неизмененными тканями.
С применением жироподавления
Диффузно-взвешенное изображение (ДВИ). Подвид МРТ обследования, позволяющий получить картину обменных процессов, происходящих на молекулярном уровне. Основывается на определении диффузии молекул воды. В патологических тканях данный процесс происходит не так, как в здоровых. Это дает дополнительную возможность отдифференцировать опухолевый очаг.
В злокачественных новообразованиях плотность клеток выше, чем в нормальной ткани, значит диффузия там уменьшена. Диффузно-взвешенные изображения оцениваются качественно (визуально) и количественно (сопоставляются с картами ИКД — измеряемого коэффициента диффузии).
МР-спектроскопия позволяет оценить биохимический состав тканей.
Мультипараметрическая МРТ(мпМРТ)
Этот метод является сочетанием стандартного T1 и T2 взвешенного изображения в различных плоскостях (саггитальной, аксиальной и фронтальной), динамического контрастирования (DCE), и получения диффузно-взвешенного изображения (DWI).
МпМРТ наиболее рекомендована в диагностике рака простаты. Она позволяет отказаться от биопсии при отсутствии МРТ-данных за злокачественное новообразование, сократить количество инвазивных обследований при выявлении латентных клинически незначимых опухолей.
Как выглядит рак предстательной железы на МРТ
При проведении мпМРТ оцениваются все полученные данные.
- На T1 ВИ хорошо видны лимфатические узлы, кровоизлияния после биопсии, костные структуры.
- Информацию о самой опухоли лучше дает T2 ВИ: РПЖ просматривается как зона со сниженным сигналом с нечеткими контурами на фоне нормальной ткани, видно прорастание опухоли за пределы капсулы железы. РПЖ исходит из периферической зоны в 70-80%, из переходной -10-20%, из центральной зоны – 1-5%.
- Динамическая МРТ с контрастированием (DCE) выявляет увеличение проницаемости сосудов в ткани опухоли, раннее накопление и более быстрое вымывание контраста.
- Диффузно взвешенные изображения: зона ограничения диффузии, яркий сигнал на ДВИ и снижение импульса на картах ИКД.

Pi—RADS (Prostate Imaging Reporting And Data System) — система оценки данных и составления заключения при визуализации простаты. Применяется для расчета вероятности выявления клинически значимого рака. Представляет собой градацию по пятибалльной шкале (1- самая низкая вероятность, 5- самая высокая). Опухоли периферической и переходной зон оцениваются по разным изображениям (периферическая – по ДВИ и ИКД, переходная – по T2 ВИ).
Заключение
Роль магнитно резонансной томографии в диагностике РПЖ возрастает. Она позволяет установить диагноз, отдифференцировать рак от простатита или аденомы, уточнить стадию, выделить клинически значимые формы карцином, избежать ненужных операций и биопсий.
В последних руководствах рекомендована мультипараметрическая МРТ для диагностики РПЖ.
Стоимость обследования колеблется от 4 до 6 тыс. рублей.
Источник rosonco.ru