Повторное развитие онкологической опухоли в предстательной железе у мужчин носит название рецидив рака простаты. Он имеет несколько видов, которые удается распознать по характерной симптоматике. Даже грамотно составленное лечение не всегда помогает предупредить появление рецидива. Вот почему даже после наступления ремиссии пациент должен регулярно посещать онколога и проходить диагностику, чтобы иметь возможность своевременно определить повторное развитие злокачественного новообразования в железистом органе.
Причины рецидива рака простаты

Возвращение к пагубным пристрастиям повышает риск вторичного возникновения недуга
По завершению лечения рака после облучения или радикальной простатэктомии может случиться рецидив заболевания. Об этом должен помнить каждый пациент, которому был поставлен данный диагноз.
Затруднительно избегать такого развития событий пациентам, которые игнорируют рекомендации своего лечащего врача. Нередко мужчины после лечения не пытаются вести здоровый образ жизни, не желают отказываться от вредных привычек. По итогу результат терапии не закрепляется, а организм слабеет.
Специалисты выделяют следующие причины рецидива рака предстательной железы:
- Инфильтрация злокачественных клеток в семенные пузырьки.
- Классификация новообразования, равная 8-10 баллам по Глисону.
- Неполное удаление опухоли.
Повлиять на появление рецидива может выбранный метод лечения рака.
Послеоперационный рецидив
Появления опухоли можно ожидать в послеоперационный период. Это значит, что рак возвращается спустя некоторое время после проведения операции по удалению злокачественного новообразования.
Несколько лет назад специалисты могли диагностировать опухоль с помощью ректального обследования прямой кишки. Сейчас же для выявления данного процесса применяются современные методики, предусматривающие использование инновационных технологий. Чаще всего послеоперационный рецидив обнаруживается благодаря результатам биопсии. К помощи данной диагностики принято прибегать в случае появления у больного следующих симптомов:
- Учащенные позывы в туалет в ночное время суток.
- Болезненные ощущения в заднем проходе и нижней части живота.
- Боли в области позвоночника.
- Расстройство мочеиспускания.
- Слабая струя во время опорожнения мочевого пузыря.
Наряду с этими симптомами у мужчины уменьшается вес тела без весомых на то причин, появляется хроническая усталость. Это могут быть клинические проявления рецидива рака простаты, с которыми обязательно нужно показаться специалисту.
Рецидив после радиотерапии
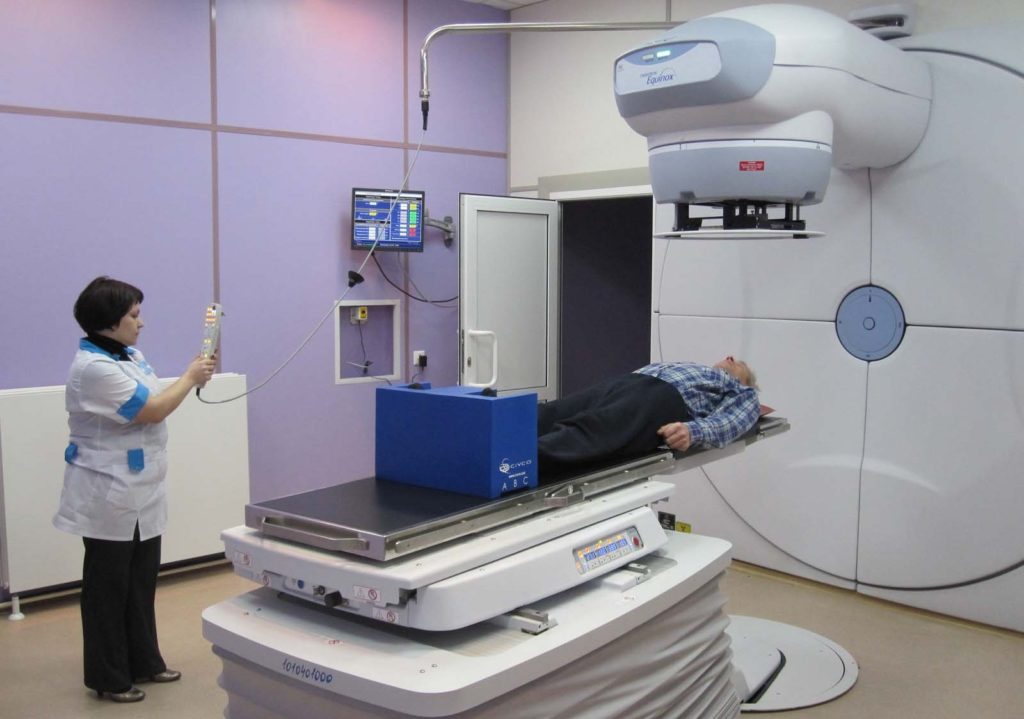
Даже современные методы порой не эффективны
После лучевой терапии вероятность рецидива рака простаты более высока, чем после хирургического вмешательства. Всего существует три основных класса повторного развития новообразования, которые отличаются друг от друга своей локализацией:
- Местный рецидив. Опухоль растет в том месте, в котором происходило облучение пораженных раком тканей. Также она может развиваться в ложе железистого органа.
- Биохимический рецидив. Патология выявляется в ходе повышения уровня ПСА.
- Системный рецидив. Злокачественное новообразование перестает быть локализованным.
Исходя из вышеуказанной информации, можно сделать вывод, что даже правильное лечение не всегда позволяет мужчине справиться с опасным заболеванием и достичь выздоровления.
Основные традиционные методы лечения рака простаты
Рецидив онкологии предстательной железы является опасным состоянием, которое нуждается в своевременной диагностике и правильном лечении. В противном случае повторное развитие злокачественной опухоли может привести к серьезным осложнениям и летальному исходу.
Существует несколько вариантов лечения онкологического новообразования в тканях предстательной железы:
- Оперативное удаление пораженного раковыми клетками органа, в данном случае, простаты.
- Лучевая терапия.
- Химиотерапия для купирования не только новообразования, но и метастазов.
После облучения или другого способа лечения рака должен вестись тщательный контроль над состоянием пациента с онкологией. Это обязательное условие независимо от того, был пройден курс радиотерапии, химиотерапии или совершено оперативное вмешательство. Соблюдение данного требования позволяет своевременно выявить рецидив рака после лучевой или другой терапии.
Тактика действий после повторного развития злокачественного новообразования зависит от того, как мужчина лечился до этого. Например, если в первый раз онколог назначил больному оперативное вмешательство, то при рецидиве ему предложат пройти курс облучения.
Как лечить рецидив
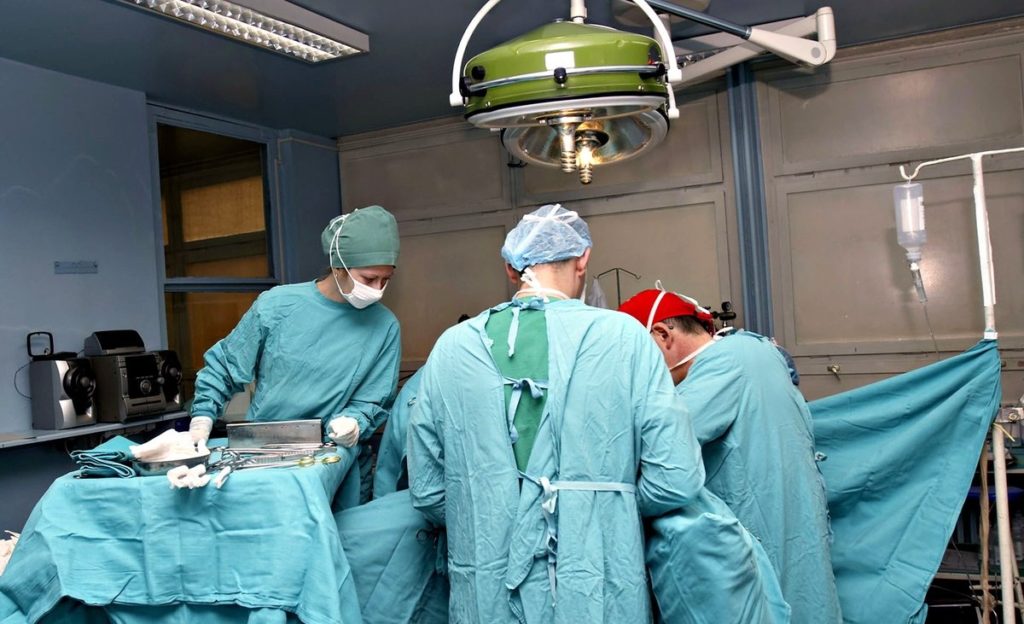
Радикальный метод не всегда нужен и подходит
Современная медицина предлагает несколько методов лечения злокачественной опухоли в предстательной железе. При таком заболевании нередко врачами предлагается оперативное вмешательство, которое позволяет удалить раковое новообразование. Но операция не во всех случаях эффективна, так как после нее в организме больного могут оставаться патогенные клетки.
После проведения лечения злокачественные клетки, оставшиеся в организме, начинают активизироваться и распространяться. Чтобы своевременно выявить данный процесс, требуется регулярно обследоваться у онколога. Лечащий врач изучит картину болезни пациента и предложит ему оптимальный вариант лечения, который, по его мнению, будет иметь благоприятный исход.
Облучение
Одним из востребованных способов лечения рецидивирующего рака простаты является лучевая терапия. Перед ее проведением пациент должен пройти тщательное обследование всего организма. Имеет смысл предлагать данный вариант терапии лишь в случае, если рак имеет локализованный характер и отсутствуют метастазы. В противном случае он не будет особо полезен больному.
Не все раковые клетки поддаются облучению. Часть из них может оставаться в первоначальном состоянии и продолжать распространяться за пределы пораженной предстательной железы. Именно поэтому лучевая терапия не особо эффективна при лечении рецидива онкологического заболевания.
Гормонотерапия
Гормонотерапия является сопутствующим способом борьбы с недугом, а не основным
Гормональная терапия практикуется в клиниках, в которых занимаются лечением онкологических заболеваний. К такому методу прибегают после проведения биохимического курса.
Онкологи не раз говорили о том, что гормональное лечение не помогает полностью избавиться от рака и его рецидива. Это лишь вспомогательная мера, которая усиливает действие других терапевтических методик, направленных на борьбу со злокачественным новообразованием в предстательной железе.
Химиотерапия
Химиотерапия обычно назначается больным, у которых биохимический или другой тип рецидива рака простаты после выявления низкой эффективности гормонального лечения. Такие меры требуются в случае, если уровень тестостерона так и не удалось понизить.
Благодаря химиотерапии состояние пациента значительно улучшается за счет облегчения болезненной симптоматики.
HIFU-терапия
Рецидив у мужчины может случиться после полного удаления предстательной железы, которая была поражена раком. В такой ситуации выходом из положения становится HIFU-терапия. Основное действие лечебного метода направлено на разрушение злокачественных клеток путем влияния на них высокосфокусированного ультразвука.
Терапия имеет ряд существенных преимуществ, которые делают данный метод лечения востребованным и эффективным. Она позволяет безболезненно справиться с рецидивирующим раком и при этом не приводит к опасным осложнениям.
Любой из существующих методов борьбы с таким заболеванием, как биохимический или другой рецидив рака предстательной железы, не дает стопроцентную гарантию купирования развития злокачественных процессов в организме мужчины. Результат терапии будет напрямую зависеть от ряда факторов, которые в момент борьбы с опухолью влияют на общее состояние пациента.
Профилактика

При наличии в анамнезе онкологического заболевания посещение пляжа категорически не рекомендовано
Каждый пациент, у которого выявлена склонность к развитию злокачественных новообразований, должен позаботиться о профилактике рака простаты и его рецидива.
Онколог во время ведения пациента должен разъяснить ему необходимость изменения образа жизни. От этого зависит успешность терапии и вероятность последующего развития онкологических опухолей.
Предупредить повторное развитие ракового заболевания у мужчин помогает регулярное соблюдение следующих профилактических мероприятий:
- Нужно отказаться от вредных привычек. В составе никотинового дыма находятся канцерогенные вещества, которые в больших количествах накапливаются в человеческом организме и способствуют развитию раковых опухолей. Не меньший вред мужчинам приносит злоупотребление спиртными напитками. Поэтому пациенты, которые не хотят в будущем столкнуться с раком, должны избавиться от пагубных привычек.
- Составление рациона на основе полезных продуктов питания. Пациентам, которые лечили рак и имеют предпосылки к его повторному развитию, настоятельно рекомендуется выбирать лечебный стол №5. Также для них подходит японская и средиземноморская диета.
- Избегать длительного нахождения под прямыми солнечными лучами. Лучше всего не загорать и по возможности прятать тело под одеждой даже в летний сезон.
- Необходимо избегать сильных нагрузок на область малого таза. Даже малейшая травма может привести к серьезным проблемам со здоровьем.
Мужчинам, которые прошли лечение рака простаты, необходимо продолжать регулярно посещать онколога в целях профилактики. Пренебрежение плановыми осмотрами у специалиста могут иметь неприятные последствия, так как из-за этого можно упустить оптимальный момент для начала борьбы с рецидивом, если он появится.
После того, как мужчина проходит курс лечения ультразвуком или облучением, ему дополнительно назначаются лекарственные препараты, с помощью которых проводится профилактика рецидива злокачественных заболеваний. Соблюдение такой схемы терапии позволяет уменьшить вероятность повторного развития рака на 20-25%.
Прогноз
Продолжительность жизни человека с раком простаты достаточно большая, если проводится адекватная терапия. Процент выживаемости может достигать 95% в случае удаления пораженного онкологией железистого органа.
Отрицательно сказывается на статистике выживаемости после заболевания раком простаты появление его рецидива. Около 15-30% пациентов с таким диагнозом ожидает летальный исход. Вторичная опухоль в 15-20% случаев сокращает жизнь мужчины. С таким заболеванием он может прожить не более 10 лет.
Источник muzhik.guru
Рецидив после радикального лечения
Риск рецидива (местного или системного) в течение 10 лет после простатэктомии или лучевой терапии составляет 27—53%. В течение 5 лет после первоначального лечения от 16 до 35% больных получают противорецидивное лечение. Ранее под рецидивом понимали опухоль, пальпируемую через прямую кишку, а также отдалённые метастазы.
Сейчас рецидивом считают рост уровня простатоспецифичного антигена (ПСА). Критерием рецидива после простатэктомии обычно считают уровень ПСА 0,2 нг/мл и более при двух последовательных измерениях. О рецидиве после лучевой терапии, согласно критериям ASTRO, можно говорить при трёх последовательных повышениях уровня простатоспецифичного антигена.
Местные и системные рецидивы
Если обнаружено повышение уровня ПСА, важно установить характер рецидива — местный или системный. После простатэктомии может идти речь о местном рецидиве, в остальных случаях — только о системном рецидиве или их сочетании. Отличить местный рецидив от системного помогает время до повышения уровня ПСА, скорость прироста и время удвоения содержания ПСА, исходный уровень его и индекс Глисона (табл. 4-9).
Таблица 4-9. Клинические и патогистологические характеристики местного и системного рецидива после радикальной простатэктомии

Увеличение уровня ПСА в первые полгода после операции обычно указывает на системный рецидив. Медиана времени удвоения уровня простатоспецифичного антигена при системных рецидивах может составлять 4,3, при местных — 11,7 мес. Скорость прироста уровня ПСА менее 0,75 нг/мл в год наблюдают у больных с местными рецидивами, более 0,7 нг/мл в год — у больных с отдалёнными метастазами.
На местный рецидив после лучевой терапии указывает медленный отсроченный рост уровня ПСА. Подтверждением местного рецидива служит положительный результат биопсии, выполненной через 18 мес после облучения и позже (при отсутствии отдалённых метастазов по данным компьютерной томографии (КТ), магнитно-резонансной томографии (МРТ) и сцинтиграфии).
Вероятность местного рецидива после простатэктомии составляет 80% при позднем подъёме уровня ПСА (более 3 лет), времени удвоения уровня ПСА более 11 мес, индексе Глисона менее 6 и стадии процесса ниже pT3aN0 и pTxR1. Вероятность системного рецидива после простатэктомии превышает 80% при раннем подъёме уровня простатоспецифичного антигена (менее одного года), времени удвоения уровня ПСА 4—6 мес, индексе Глисона 8—10, стадии рТ3b и pTxN1.
Местный рецидив после лучевой терапии и HIFU диагностируют при положительном результате биопсии при отсутствии отдалённых метастазов. Биопсия предстательной железы показана лишь отдельным больным при планировании повторного местного лечения (например, простатэктомии или повторного сеанса HIFU).
Обследование при подозрении на рецидив
Для подтверждения рецидива при повышении уровня ПСА обычно проводят физикальное обследование, УЗИ, КТ или МРТ малого таза, биопсию ложа опухоли и области анастомоза. При отсутствии симптомов эти исследования редко обнаруживают опухоль, так как рост уровня ПСА обычно происходит за 6—48 мес до явного рецидива.
Пальцевое ректальное исследование при нулевом или очень низком уровне ПСА обычно не приносит результатов. При повышении уровня простатоспецифичного антигена назначают МРТ малого таза, КТ брюшной полости и сцинтиграфию костей, но из-за низкой чувствительности и специфичности при раннем рецидиве эти исследования малоинформативны. При подъёме уровня ПСА после простатэктомии результат сцинтиграфии положителен лишь у 4,1% больных. Вероятность положительного результата сцинтиграфии не превышает 5%, пока уровень ПСА не достигнет 40 нг/мл.
Средний уровень ПСА, при котором сцинтиграфия обнаруживает метастазы, должен превышать 60 нг/мл, а скорость прироста уровня ПСА — 22 нг/мл в год. Уровень и скорость прироста содержания простатоспецифичного антигена позволяют предсказать результат сцинтиграфии, а скорость прироста уровня ПСА — результат КТ. Таким образом, при уровне ПСА менее 20 нг/мл или скорости прироста содержания ПСА менее 20 нг/мл в год сцинтиграфия и КТ не приносят дополнительной информации. Эндоректальная МРТ обнаруживает местный рецидив у 81% больных со средним уровнем ПСА 2 нг/мл. ПЭТ рекомендуют для ранней диагностики рецидивов различных опухолей.
Сцинтиграфия с антителами к простатическому мембранному антигену (простасцинт) — один из новых методов обнаружения рецидивов. Его диагностическая точность достигает 81%. Независимо от уровня простатоспецифичного антигена метод обнаруживает возникновение рецидива у 60—80% больных, что может помочь при выборе тактики лечения. Сцинтиграфия с этими антителами положительна у 72 из 255 больных с уровнем ПСА 0,1—4 нг/мл после простатэктомии, причём накопление изотопа наблюдают при любом уровне ПСА.
Биопсия зоны анастомоза позволяет обнаружить рецидив только у 54% больных. Лишь при наличии пальпируемого или гипоэхогенного образования вероятность положительного результата приближена к 80%. Существует чёткая зависимость между этим показателем и уровнем ПСА: при содержании ПСА менее 0,5 нг/мл результат положителен у 28% больных, при уровне простатоспецифичного антигена более 2 нг/мл — у 70% больных. Учитывая эти данные, биопсию из зоны анастомоза обычно не берут и ориентируются на уровень ПСА и скорость его удвоения. Кроме того, выживаемость при доказанных рецидивах примерно такая же, как при регистрации изолированного повышении ПСА.
Согласно рекомендациям ASTRO, при повышении уровня ПСА после лучевой терапии биопсия предстательной железы не показана. Впрочем биопсия имеет ключевое значение для решения вопроса о простатэктомии или HIFU у таких больных. После лучевой терапии (дистанционной или брахитерапии) биопсию обычно проводят не ранее чем через 18 мес после криодеструкции или через 6 мес после ультразвуковой деструкции.
Клинические рекомендации по обследованию при подозрении на рецидив
Лечение рецидивов после радикальной простатэктомии
Гормонотерапия
При высоком дооперационном уровне ПСА (более 20 нг/м, индексе Глисона более 7, нерадикальной операции и местнораспространённых опухолях pT3b, pTхN1) целесообразна ранняя гормонотерапия. Однако её влияние на выживаемость до сих пор не установлено. При ранней гормонотерапии метастазы возникают реже, чем при отсроченной, выживаемость в обоих случаях примерно одинаковая. Необходимость гормонотерапии подтверждает испытание MRC, в котором рецидив был отмечен у всех больных, получивших лучевую терапию по поводу роста уровня ПСА после простатэктомии при опухолях pT3b, pTxN1 и индексе Глисона 8.
Монотсрапию антиандрогенными препаратами больные переносят лучше, чем комбинированную (реже возникают приливы, снижение потенции, утрата полового влечения), однако антиандрогены вызывают гинекомастию и боль в сосках. У больных без отдалённых метастазов бикалутамид (по 150 мг/сут) достоверно снижает риск прогрессирования заболевания. Таким образом, антиандрогены могут быть альтернативой кастрации при повышении уровня простатоспецифичного антигена после радикального лечения (особенно у относительно молодых больных без сопутствующих заболеваний).
Наблюдение
Динамическое наблюдение обычно проводят при индексе Глисона менее 7, позднем (через 2 года после операции) повышении уровня ПСА и времени его удвоения более 10 месяцев. В таких случаях медиана времени до возникновения метастазов составляет 8 лет, а медиана времени от возникновения метастазов до наступления летального исхода — ещё 5 лет. HIFU-терапия
В последнее время появляется всё больше данных о результатах HIFU-терапии местного рецидива после РПЭ. Чаще всего рецидив обнаруживают при ТРУЗИ и подтверждают гистологически (биопсия). Тем не менее HIFU-терапия лишь отодвигает сроки назначения гормонотерапии. Точные данные о выживаемости отсутствуют.
Клинические рекомендации по лечению рецидива после простатэктомии
Лечение рецидива после лучевой терапии
Наиболее часто больные с рецидивом после лучевой терапии получают гормонотерапию (до 92%). Без лечения время от повышения уровня ПСА до манифестации рецидива составляет около 3 лет. Кроме гормонотерапии при рецидиве после облучения возможно и местное лечение — простатэктомия, HIFU-терапия, криотерапия, брахитерапия. Простатэктомия не нашла широкого применения из-за частых осложнений (недержание мочи, повреждение прямой кишки), а также из-за высокого риска местного рецидива. Однако при тщательном отборе больных эта операция может обеспечить длительный безрецидивный период.
По последним данным, 5-летняя безрецидивная выживаемость после лучевой терапии соответствует таковой после первичной простатэктомии, проведённой на тех же стадиях заболевания, 10-летняя выживаемость составляет 60—66%. В течение 10 лет от прогрессирования опухоли умирают 25—30% больных. При локализованных опухолях, отсутствии опухолевых клеток в крае резекции, инвазии семенных пузырьков и метастазирования в лимфатические узлы безрецидивная выживаемость достигает 70—80% по сравнению с 40—60% при местнораспространённых опухолях.
Простатэктомия при местном рецидиве оправдана при отсутствии тяжёлых сопутствующих заболеваний, ожидаемой продолжительности жизни не менее 10 лет, опухолях Т1-2, индексе Глисона менее 7 и уровне простатоспецифичного антигена менее 10 нг/мл. В остальных случаях до операции сложно определить распространённость опухоли, что повышает риск передней или тотальной экзентерации, осложнений, а также повторного рецидива.
Рекомендовано динамическое наблюдение за больными с вероятным местным рецидивом (из группы низкого риска, с поздним рецидивом и медленным ростом уровня ПСА), настроенными против повторного радикального лечения. Ретроспективный анализ не обнаружил преимуществ гормонотерапии по сравнению с динамическим наблюдением при времени удвоения уровня ПСА более 12 мес: 5-летняя выживаемость без метастазирования составила 88% при гормонотерапии и 92% — на фоне наблюдения.
Клинические рекомендации по лечению рецидива после лучевой терапии
Таблица 4-10. Клинические рекомендации по лечению рецидивов после радикального лечения

Качество жизни при лечении больных локализованным раком предстательной железы
В современной литературе большое внимание уделяют проблеме качества жизни у пациентов с раком предстательной железы после завершения лечения. Все современные методы лечения рака предстательной железы (РПЖ) влекут за собой серьезные и продолжительные осложнения, в то время как выделить наиболее эффективный метод среди прочих в настоящее время невозможно. Для большинства онкологических заболеваний 5-летняя выживаемость нередко служит показателем излечения, в то время как смертность от локализованного РПЖ в первые 5 лет, наоборот, явление нечастое.
Таким образом, значительная ожидаемая продолжительность жизни диктует необходимость учёта мнения пациента при выборе лечебной тактики, а последствия лечения не должны быть тяжелее самого заболевания. В связи с этим всё большее внимание в последние годы уделяют не только эффективности метода лечения, но и его влиянию на качество жизни пациента.
Качество жизни, связанное со здоровьем
Понятие «качество жизни» тесно связано с определением здоровья, принятым Всемирной организацией здравоохранения. В его рамках рассматривают не только физические, но и психические и социальные аспекты жизнедеятельности человека. В более узких медицинских рамках используют понятие «качество жизни, связанное со здоровьем» (health-related quality of life), не рассматривающее культурные, социальные или политические факторы и позволяющее акцентировать внимание на влиянии заболевания и его лечения на качество жизни пациента.
Качество жизни зависит от личностных качеств пациента, внутреннего восприятия заболевания, психологического благополучия, степени выраженности симптомов заболевания и/или последствий его лечения. Все эти компоненты формируют персональное представление пациента о его болезни, порой отличное от видения врача. Практика показывает, что отсутствие инструментально регистрируемых отклонений не умаляет значимости субъективного восприятия пациента и далеко не всегда соответствует последнему.
Сравнительная характеристика влияния современных методов лечения локализованного рака предстательной железы на качество жизни
Сложность выбора способа лечения локализованного РПЖ объясняют недостатком рандомизированных сравнительных исследований трёх основных методов: радикальной простатэктомии (РПЭ), дистанционной лучевой терапии и брахитерапии. Помимо изучения эффективности каждого из методов, важна оценка их влияния на качество жизни пациентов, поскольку именно оно нередко служит ключевым фактором в выборе определённой лечебной стратегии.
Использование опросника SF-36 показало преимущества РПЭ перед дистанционной лучевой терапией и брахитерапией. В течение первого месяца наблюдают существенный спад показателя QoL, характеризующего более тяжёлый послеоперационный период, однако уже через 4 мес отмечают его повышение до исходного уровня. Необходимо отметить, что исходный показатель QoL у пациентов, которым выполнена радикальная простатэктомия, на 7—10 пунктов выше, чем в других группах. Это объясняют тем, что возраст пациентов, выбравших оперативное лечение, в среднем на 6 лет меньше.
Несмотря на невысокую частоту послеоперационных осложнений, наименее предпочтительным методом с точки зрения влияния на качество жизни считают брахитерапию (диаграмма 4-1). В сравнении с контрольной группой (пациенты без лечения) после брахитерапии наблюдали расстройства мочеиспускания (ирритативные симптомы и уменьшение объёмной скорости мочеиспускания), сексуальной функции, нарушения со стороны желудочно-кишечного тракта.

Диаграмма 4-1. Динамика показателя общего качества жизни после различных методов лечения локализованного рака предстательной железы
При применении дистанционной лучевой терапии на первый план выходят признаки лучевого поражения кишечника: диарея, кровотечения, обструкция. Часто происходит поражение прямой кишки: нередко наблюдают недержание кала вследствие лучевого поражения нервов, иннервирующих анальный сфинктер. Тот же механизм лежит в основе развития эректильной дисфункции.
У пациентов, которым выполнена радикальная простатэктомия, обнаруживают недержание мочи и сексуальные расстройства, однако в целом качество жизни считают самым высоким именно после оперативного лечения. Это можно объяснить тем, что операция — единственный гарантированный способ удаления локализованной опухоли, что даёт дополнительный психологический стимул для преодоления трудностей, связанных с послеоперационными осложнениями (диаграмма 4-2).

Диаграмма 4-2. Сравнительная характеристика влияния различных методов лечения рака предстательной железы на качество жизни пациентов
Расстройства мочеиспускания у пациентов после радикальной простатэктомии
Среди расстройств мочеиспускания после радикальной простатэктомии доминирует недержание мочи. Согласно исследованию Каракевич и соавт. (2000), именно это осложнение — основной фактор снижения качества жизни после радикальной простатэктомии. Его встречают в 15—60% случаев. Такой большой диапазон величин объясняют тем, что во многих случаях недержание мочи — временное явление, проходящее самостоятельно по прошествии нескольких недель или месяцев.
В отличие от нервосохраняющего варианта, применение традиционной методики РПЭ вдвое увеличивает продолжительность периода восстановления функции сфинктерного аппарата мочевого пузыря. Другой важный фактор, влияющий на частоту недержания мочи, — возраст пациента. Частота продолжительного недержания мочи (более двух лет) у больных в возрасте 60—69 лет составляет 5—10%, у пациентов старше 70 лет — 15%.
Только 61% пациентов через год после лечения способны удерживать мочу на дооперационном уровне, однако уже через 6 мес 90% пациентов не используют прокладок (диаграмма 4-3). Таким образом, несмотря на сохранение функциональных нарушений со стороны сфинктерного аппарата через 6 мес после операции, это не доставляет пациентам существенного беспокойства.

Диаграмма 4-3. Динамика отмечаемых пациентами симптомов нарушения мочеиспускания в течение 2 лет после радикальной простатэктомии
В случае сохранения недержания мочи в течение продолжительного периода возможно выполнение инъекций коллагена или имплантация искусственного сфинктера, однако к подобным мерам прибегают лишь 3% пациентов. Важно отметить, что наиболее продолжительное недержание мочи наблюдают у пациентов, отмечавших подобную симптоматику до операции.
Сексуальные расстройства после радикальной простатэктомии
Импотенция (эректильная дисфункция) — частое осложнение РПЭ, существенно влияющее на качество жизни пациентов. Это подтверждает тот факт, что многие мужчины при выборе метода лечения РПЖ ориентированы не на ббльшую ожидаемую продолжительность жизни, а на сохранение потенции. Подавляющее большинство пациентов сталкиваются с этой проблемой в первые месяцы после операции. Последующее восстановление нормальной половой функции вариабельно и зависит от наличия сексуальных расстройств до операции, гормонального статуса, применения нервосберегающей методики радикальной простатэктомии.
Однако даже при сохранении сосудисто-нервных пучков восстановление эректильной функции может занять месяцы и даже годы. Считают оправданным усиление эрекции с помощью применения медикаментозных средств: таблетированных ингибиторов фосфодиэстеразы-5, уретральных суппозиториев, интракавернозных инъекций препаратов простагландина, а также использования вакуумных устройств. Высокоэффективным методом коррекции эректильной дисфункции считают эндопротезирование полового члена.
К сожалению, у большинства мужчин в возрасте 65 лет и старше не происходит полное самостоятельное восстановление эректильной функции по сравнению с дооперационным уровнем, однако значительное количество пациентов адаптируются или применяют вышеуказанные средства для достижения удовлетворительного уровня половой активности.
Более молодые пациенты (40—60 лет) после выполнения нервосберегающей РПЭ значительно чаще способны к осуществлению полноценного полового акта без применения какой-либо дополнительной терапии. Талькотт и соавт. (1997) показали, что, несмотря на меньшую частоту эректильной дисфункции после выполнения нервосберегающей радикальной простатэктомией по сравнению с традиционной методикой, уровень неудовлетворённости сексуальной активностью у таких пациентов одинаков.
Практика показывает, что сексуальные нарушения доставляют пациентам значительно меньше неудобств, нежели расстройства мочеиспускания (диаграмма 4-4). Это можно объяснить пожилым возрастом пациентов, многие из которых не жили половой жизнью до операции, а отсутствие эрекции в послеоперационном периоде не влияет негативно на качество их жизни. По данным исследований, 75% пациентов удовлетворены или адаптировались к послеоперационным изменениям сексуальной функции, полноценную эрекцию отмечают только 12% больных. Этот факт необходимо учитывать при выборе метода лечения.

Диаграмма 4-4. Динамика отмечаемых пациентами сексуальных нарушений в течение 2 лет после радикальной простатэктомии
Неоадъювантная гормональная терапия и качество жизни
В настоящее время вопрос о необходимости проведения неоадъювантной гормональной терапии перед РПЭ пациентам с локализованным РПЖ остаётся открытым. Многочисленные исследования показали, что применение неоадъювантной гормонотерапии не увеличивает продолжительность жизни и существенно не снижает риск рецидива после операции. В то же время длительное её применение (более 6 мес) приводит к снижению качества жизни; ухудшению общего самочувствия, возникновению приливов, снижению либидо и сексуальной функции.
С другой стороны, применение агонистов гонадолиберина (трипторелин) коротким курсом до 3 мес позволяет существенно уменьшить объём предстательной железы, поскольку её значительные размеры усложняют проведение оперативного вмешательства. Кроме того, лечение трипторелином способствует уменьшению интраоперапионной кровопотери.
Важно отметить, что назначение трипторелина коротким курсом не вызывает существенного снижения либидо и половой функции, больные легко его переносят. Кроме того, применение трипторелина позволяет отсрочить операцию (без риска прогрессирования заболевания) и выбрать максимально удобное время для её проведения. Решение о назначении длительного курса принимают в индивидуальном порядке. Оно показано при высоком риске местного распространения опухоли.
Источник medbe.ru
Рецидив после лучевой терапии
Рецидив после лучевой терапии
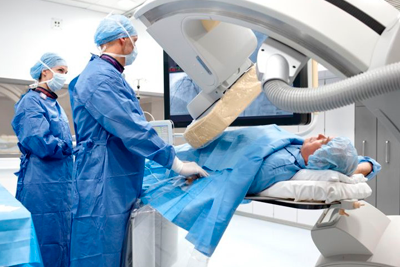
Хирургические и терапевтические методы лечения онкологических заболеваний не обладают абсолютной эффективностью, поэтому даже после проведения всех необходимых манипуляций возможно возвращение болезни. Рецидив после лучевой терапии может быть результатом неполного лечения или естественным осложнением патологии. Зачастую ионизирующее облучение назначают после оперативного вмешательства, однако такой метод не уничтожает всех злокачественных клеток. Врачебная консультация поможет пациенту узнать больше о такой процедуре, как лучевая терапия: рецидивы, способы проведения, эффективность, осложнения и другие аспекты.
Информация о методе
Лучевую терапию также называют радиационной или ионизирующей терапией. Это один из самых эффективных методов лечения онкологических заболеваний, подразумевающий воздействие радиации на пораженные ткани. Результатом применения такой процедуры является предотвращение дальнейшего роста и распространения злокачественной опухоли. Иногда лучевая терапия также позволяет добиться уменьшения размера патологического очага. В зависимости от показаний радиация применяется в качестве главного метода лечения или адъювантной терапии. Рецидив после лучевой терапии возможен, однако при корректном применении риск такого исхода минимален.
В радиационной терапии применяются разные типы воздействия, включая корпускулярное и волновое излучение. При этом независимо от вида терапии основной механизм воздействия связан с поражением генетической информации клеток. Благодаря влиянию ионизирующего излучения в злокачественных клетках формируются молекулы, разрывающие связи в ДНК. Результатом такого воздействия является неспособность аномальных клеток к дальнейшему делению и выполнению функций. Метод не обладает абсолютной селективностью, однако основное действие приходится именно на злокачественные ткани из-за особенностей их метаболизма.
Лучевая терапия редко является основным методом лечения. Обычно первой назначаемой процедурой является операция, во время которой врач удаляет патологический очаг. Уже после хирургии проводится терапевтическое лечение, что включает и радиационную терапию. В этом случае процедура помогает уничтожить рассеянные в организме злокачественные клетки и предотвратить повторный рост опухоли. Тем не менее иногда лучевая терапия применяется в качестве первичного метода. В частности, неоадъювантная лучевая терапия может быть показана при неоперабельной опухоли или поздней стадии онкологического заболевания.
Главным недостатком ионизирующего облучения опухолевой ткани является высокий риск возникновения побочных эффектов. Негативные последствия связаны с воздействием радиации на здоровые ткани. Облучение может не только нарушить функции органов, но и спровоцировать возникновение генетических мутаций в клетках. Врачам также известно, что проведение лучевой терапии является фактором риска возникновения нового онкологического заболевания. Современные точечные способы применения радиации значительно уменьшают риск возникновения осложнений, однако процедура все еще считается достаточно опасной.
Показания и противопоказания
Основным показанием к прохождению лучевой терапии является наличие злокачественной опухоли в любой ткани. В зависимости от размера, формы и стадии патологии онколог может назначить терапию как основное средство лечение или в качестве вспомогательной процедуры.
Возможные цели назначения:
- Первичное лечение неоперабельных и крупных злокачественных новообразований, включая рак терминальной стадии.
- Метод подготовки к оперативному вмешательству, заключающийся в попытке уменьшения размера опухоли.
- Уничтожение оставшихся в организме аномальных клеток после операции.
- Часть комплексной терапии онкологии, включающей медикаментозное противоопухолевое лечение.
- Часть паллиативной терапии на поздних стадиях, необходимой для облегчения симптомов болезни.
Относительные и абсолютные противопоказания:
- Выраженная онкологическая кахексия, не позволяющая провести лечение.
- Туберкулез.
- Тяжелые расстройства деятельности сердечно-сосудистой системы, почек и печени.
Несмотря на то, что рецидивы рака после лучевой терапии всегда возможны, без этой процедуры редко обходится лечение злокачественных новообразований. Так, например, врачи нередко обнаруживают рецидив рака гортани после лучевой терапии, однако проведение дополнительного лечения помогает устранить опухоль.
Виды и побочные эффекты
Радиационная терапия классифицируется по виду излучения, дозировке и методу воздействия. Наиболее важным критерием является область применения ионизирующего излучения, от которой зависит риск возникновения осложнений.
- Контактная терапия, подразумевающая непосредственное воздействие радиации на злокачественную опухоль. Такая процедура может быть проведена во время оперативного вмешательства или при поверхностных новообразованиях. Риск осложнений значительно ниже, чем при других видах процедуры.
- Дистанционная терапия, при которой радиация преодолевает здоровые ткани. Это основной способ воздействия при злокачественных опухолях внутренних органов. Точечное применение помогает уменьшить нагрузку на здоровые ткани.
- Радионуклидная терапия – селективное воздействие радиации в патологическом очаге.
Рецидив после лучевой терапии является не единственным возможным негативным последствием процедуры. Непосредственно во время облучения в организме происходят патологические процессы, обуславливающие возникновение побочных эффектов. Важно понимать, что быстрое деление злокачественных клеток делает их более приемлемой мишенью для радиации, однако невозможно полностью избежать повреждения здоровых клеток.
Распространенные побочные эффекты:
- Выпадение волос, раздражение кожи и ломкость ногтей.
- Усталость и слабость.
- Сухость во рту и выделение вязкой слюны.
- Нарушение глотания.
- Боль в горле и изменение вкуса пищи.
- Тошнота и рвота.
- Кашель и одышка.
- Диарея или запор.
- Раздражение мочевого пузыря, частое мочеиспускание.
- Эректильная дисфункция.
- Нарушение работы иммунитета и частое возникновение инфекционных заболеваний.
Многие осложнения сохраняются в течение нескольких месяцев и даже лет после проведения терапии.
Почему возникает рецидив после лучевой терапии?
Онкологическими заболеваниями называют злокачественные опухоли, образующиеся в определенных тканях и органах. Сами по себе опухоли являются патологическими структурами клеточного строения, отличающимися особенностями обмена веществ и деления от близлежащих тканей. Опухоли быстро увеличиваются в размере, повреждают органы и распространяются в другие области. На поздних стадиях злокачественные клетки проникают в кровоток и лимфу, что приводит к формированию вторичных новообразований в отдаленных органах.
В отличие от хирургического лечения, необходимого для полного уничтожения опухоли, терапия имеет более сложный механизм воздействия. Большинство применяемых процедур направлено уничтожение определенных клеток в организме, отличающихся от здоровых тканей. Химиотерапия поражает ДНК и вызывает клеточную смерть, а лучевая терапия останавливает распространение новообразований. Тем не менее даже при стойкой ремиссии на фоне лечения возможно возвращение заболевания.
Чаще всего рецидив после лучевой терапии обусловлен сохранением отдельных злокачественных клеток в лимфатической системе или тканях, не подвергшихся воздействую ионизирующего излучения. На 3 стадии онкологического процесса аномальные клетки часто проникают в лимфоузлы, в результате чего возникает риск распространения болезни. На поздних стадиях даже при полном удалении очага болезни и облучении сохраняется риск рецидива. Решением такой проблемы может быть регулярная диагностика после проведения лечения и профилактика роста новых опухолей.
Предварительная диагностика
Перед назначением лучевой терапии пациенту требуется консультация врача и диагностика. На приеме онколог спрашивает больного о жалобах, изучает анамнестические данные и проводит физикальное обследование. Следующим этапом диагностики является назначение инструментальной и лабораторной диагностики. Результаты тестов помогут врачу определить форму и стадии онкологического процесса, что очень важно для подбора метода радиационной терапии.
- Анализ крови на онкологические маркеры, биохимию и общие показатели.
- Ультразвуковое обследование – визуализация внутренних органов с помощью высокочастотных звуковых волн.
- Рентгенография – первичный метод сканирования, позволяющий получить снимок пораженного органа.
- Компьютерная и магнитно-резонансная томография – высокоточные методы сканирования, дающие врачу возможность получить уточненные изображения органов и тканей. Результаты КТ и МРТ также необходимы для поиска метастазов.
- Эндоскопическое обследование.
- Биопсия опухолевой ткани – основной способ лабораторной диагностики, позволяющий исследований аномальные клетки. Результаты биопсии необходимы для определения гистологической формы онкологии.
Во время диагностики врач также исключает наличие противопоказаний и уточняет локализацию опухоли для проведения точечного облучения.
Таким образом, рецидив после лучевой терапии является возможным негативным последствием лечения. Консультация онколога поможет пациенту узнать больше о рисках противоопухолевой терапии.
Источник mosonco.ru